Imaginez un monde coupé du nôtre depuis des millions d'années, où le temps semble suspendu et où la vie a évolué selon des règles que nous commençons à peine à soupçonner. Dans les entrailles de la Terre, loin de la lumière du soleil et de toute influence humaine, se cache un écosystème d'une complexité vertigineuse. Ce qui s'y passe remet en cause l'une de nos plus grandes certitudes médicales : l'efficacité de nos armes chimiques contre les infections. Bienvenue dans la grotte de Lechuguilla, un laboratoire naturel où les bactéries ont développé des stratégies de défense qui rendent nos antibiotiques modernes obsolètes. ! Intérieur d'une grotte de glace contrastant avec la lumière du jour et la présence de trois silhouettes humaines.
Lechuguilla : plus d'humains ont foulé le sol lunaire que le fond de cette grotte

Située dans l'État américain du Nouveau-Mexique, au cœur du parc national de Carlsbad Caverns, la grotte de Lechuguilla n'est pas une simple cavité touristique. Il s'agit d'un labyrinthe souterrain titanesque qui s'étend sur plus de 242 kilomètres de galeries développées, plongeant jusqu'à 489 mètres de profondeur sous la surface. C'est l'un des systèmes karstiques les plus profonds et les plus longs des États-Unis, un monde féerique sculpté par l'acide sulfurique où les cristaux de gypse forment des colonnes géantes aussi fragiles que spectaculaires. Là, à 400 mètres sous terre, des lacs d'une eau étrangement verte parsèment le paysage, créant une atmosphère digne d'une œuvre de science-fiction.
Cependant, la beauté des lieux n'est que la face visible d'un isolement absolu. La grotte est protégée par une couche de grès imperméable qui agit comme un couvercle hermétique, scellant cet environnement du reste de la planète. Il faut environ 1 000 ans pour qu'une simple goutte d'eau de surface s'infiltre à travers la roche et atteigne les profondeurs de la cavité. En raison de cette fragilité extrême et de la difficulté technique d'accès, l'entrée est formellement interdite au public. Seule une poignée de chercheurs et de spéléologues hautement qualifiés a foulé le sol de ses parties les plus reculées, faisant dire que davantage d'êtres humains ont marché sur la Lune que dans certaines zones profondes de Lechuguilla.
Un labyrinthe de 242 kilomètres scellé sous les montagnes Guadalupe ! La grotte de Lechuguilla et ses formations géologiques spectaculaires.
La formation géologique de Lechuguilla est une histoire qui défie l'imagination et les modèles classiques de spéléogenèse. Contrairement à la plupart des grottes qui se forment par dissolution du calcaire par l'eau de pluie chargée d'acide carbonique, Lechuguilla est née d'une réaction chimique violente survenue il y a des millions d'années. Du sulfure d'hydrogène, migrant depuis des gisements de pétrole voisins, a réagi avec l'eau oxygénée pour créer de l'acide sulfurique. Cet acide puissant a rongé la roche calcaire, creusant des espaces titanesques du bas vers le haut, laissant derrière lui des cavernes aux formes éthérées et des dépôts de gypse massifs.
Cette origine chimique unique a créé une frontière physique quasi infranchissable. La roche de grès située au-dessus de la cavité empêche toute contamination rapide venant de la surface. Pour un scientifique, cet isolement est une aubaine inespérée : c'est l'équivalent d'une capsule temporelle biologique. Les organismes qui y vivent sont les descendants de lignées qui ont évolué séparément du reste de la biosphère terrestre depuis des éons, offrant un aperçu rare de la vie telle qu'elle pouvait être bien avant l'apparition de l'humanité.
Pas de lumière, pas d'oxygène, pas de contact avec la surface : les règles de la vie souterraine
Dans cet univers clos, les règles classiques de la biologie de surface s'effondrent. Ici, il n'y a pas de photosynthèse, pas de plantes vertes, pas de chaîne alimentaire basée sur le soleil. La vie, si elle veut exister, doit se contenter des ressources minérales disponibles. Les organismes qui survivent dans ces profondeurs sont qualifiés d'extrêmophiles, capables de prospérer dans des conditions qui seraient mortelles pour la majorité des êtres vivants. À Lechuguilla, les bactéries ont développé des mécanismes fascinants pour puiser leur énergie directement dans la roche. ! Exploration verticale de la grotte de Veryovkina.
On y trouve des communautés microbiennes qui se nourrissent de minéraux comme le soufre, le fer et le manganèse. Ces chimiotrophes oxydent ces composés inorganiques pour produire l'énergie nécessaire à leur survie, vivant dans un quasi-jeûne permanent, loin de toute dépendance au monde extérieur. Cet isolement rigoureux pose une question scientifique vertigineuse : comment des organismes qui n'ont jamais été exposés à l'homme ou à ses médicaments peuvent-ils développer des résistances à nos antibiotiques les plus modernes ?

« Foncer, attraper, poignarder » : la chasse sanglante des bactéries des profondeurs
Contrairement à l'image stéréotypée d'un désert biologique stérile, la grotte de Lechuguilla regorge d'une vie microscopique intense et brutale. Loin d'être un havre de paix, cet environnement est une arène où chaque microbe lutte pour sa survie. La scientifique Hazel Barton, professeure de sciences biologiques et spéléologue chevronnée, étudie ces écosystèmes souterrains depuis plus de deux décennies. Ses travaux ont révélé que les interactions entre ces organismes unicellulaires sont d'une violence inouïe, rappelant les prédations que l'on observe dans les jungles les plus denses de la surface.
C'est dans ce contexte que les découvertes sur la résistance aux antibiotiques prennent tout leur sens. Ce n'est pas une anomalie fortuite, mais le résultat de millions d'années de guerre biologique. Hazel Barton utilise une métaphore frappante pour décrire ce qui se passe sous nos yeux à l'échelle microscopique : dans ces ténèbres, les bactéries ne sont pas des passives, mais des prédatrices actives qui traquent, attaquent et dévorent leurs concurrentes avec une précision chirurgicale.
Hazel Barton et la jungle invisible à 400 mètres sous terre
Hazel Barton, de l'Université de l'Alabama, est une figure centrale de la compréhension de ce monde caché. Sa double compétence en spéléologie et en microbiologie lui permet d'accéder à des environnements que peu de chercheurs peuvent atteindre. Pour elle, la grotte de Lechuguilla fonctionne exactement comme une forêt tropicale, mais à une échelle microscopique. Il existe une structure sociale complexe, une hiérarchie, et surtout des relations de prédation élaborées qui régulent les populations microbiennes.
Selon ses observations, ce milieu souterrain est densément peuplé. Dans chaque goutte d'eau ou chaque film minéral sur les parois, des millions de bactéries interagissent. Mais contrairement à ce que l'on pourrait penser, cette cohabitation n'est pas pacifique. Comme dans une jungle, il y a des prédateurs et des proies. Cette dynamique de chasse constante crée une pression sélective énorme, forçant les organismes à développer des armes de plus en plus sophistiquées pour survivre. C'est cette « jungle invisible » qui a servi de creuset à l'évolution des mécanismes de résistance que nous observons aujourd'hui. ! Un chercheur en laboratoire manipulant des échantillons avec une pipette et une microplaque.

Des poils harpons et des enzymes : l'arsenal meurtrier des bactéries prédatrices
La description faite par Hazel Barton des comportements prédateurs dans la grotte est d'une violence littérale. Elle explique avoir observé des bactéries qui « foncent pour attraper, poignarder et tuer » d'autres microbes. Ces prédateurs microscopiques sont équipés d'organites spécialisés qui fonctionnent comme des harpons biochimiques. Ils projettent des structures cellulaires pour agripper leurs proies, perçant leurs membranes cellulaires pour injecter des enzymes mortelles.
Ces enzymes, ou toxines, ont pour fonction de digérer la proie de l'intérieur, permettant au prédateur d'absorber les nutriments libérés. C'est un combat quotidien, impitoyable, où seule l'innovation génétique garantit la survie. Si une proie développe un bouclier, le prédateur doit inventer une nouvelle arme ; si le prédateur invente une nouvelle toxine, la proie doit développer une résistance. C'est cette course à l'armement perpétuelle, isolée du reste du monde depuis 4 millions d'années, qui a abouti à la création de molécules capables de vaincre des défenses chimiques complexes. Les bactéries de Lechuguilla ne se contentent pas de résister aux poisons ; elles en fabriquent pour éliminer leurs rivaux.

Paenibacillus LC231 : résistante à 26 antibiotiques sur 40, isolée depuis 4 millions d'années
Au cœur de ce laboratoire naturel, une découverte en particulier a secoué la communauté scientifique. Les chercheurs ont isolé une souche bactérienne spécifique, baptisée Paenibacillus sp. LC231, dans les sols profonds de la grotte. Cette bactérie, totalement inoffensive pour l'homme, détient un record effrayant : elle résiste naturellement à 26 des 40 antibiotiques modernes testés par les scientifiques. Plus alarmant encore, elle parvient à inactiver sept classes distinctes d'antibiotiques, incluant des médicaments de dernier recours comme la daptomycine, utilisée en hôpital pour traiter les infections mortelles au staphylocoque doré résistant à la méthicilline (MRSA).
Les études publiées, notamment dans la revue PLoS ONE en 2012 et plus tard dans Nature Communications en 2016, ont permis de décortiquer le génome de cette survivante. L'analyse de 93 souches bactériennes prélevées dans la grotte a révélé que la résistance aux antibiotiques n'était pas une exception, mais la norme dans cet environnement. Ces organismes n'ont jamais vu un être humain, et encore moins une pilule antibiotique, et pourtant, ils sont immunisés contre nos meilleures armes chimiques. ! Détail microscopique de bactéries colorées en jaune au sein de structures cellulaires hôtes bleues.
L'étude de 2012 : 93 souches, un verdict sans appel
L'étude menée en 2012 a marqué un tournant dans notre compréhension de la résistance antimicrobienne. En examinant 93 souches bactériennes isolées de différents secteurs de la grotte de Lechuguilla, l'équipe de recherche a constaté que la majorité d'entre elles présentaient une résistance à plusieurs antibiotiques. Certains microorganismes étaient capables de supporter l'exposition à 14 antibiotiques commerciaux différents. Le plus troublant est que ces souches ont été isolées de zones qui n'ont pas été en contact avec la surface depuis environ 4 millions d'années.
Ce résultat a servi de preuve irréfutable que la résistance aux antibiotiques est un phénomène naturel, ancien et largement répandu, indépendamment de l'activité humaine. Avant même qu'Alexander Fleming ne découvre la pénicilline en 1928, les bactéries de Lechuguilla se battaient déjà avec des molécules similaires ou avaient développé des défenses contre elles. Cela nous force à admettre que ce que nous considérions comme une adaptation moderne aux médicaments est en réalité un héritage évolutif profondément ancré dans le monde microbien.
LC231 contre la daptomycine : quand une bactérie non pathogène bat notre arme de dernier recours
La daptomycine est souvent perçue comme le « dernier rempart » contre les infections bactériennes résistantes qui ravagent les hôpitaux. Son mécanisme d'action est complexe et spécifique, ce qui rend le développement d'une résistance très difficile pour les bactéries pathogènes classiques. Pourtant, l'analyse de Paenibacillus LC231 a révélé qu'elle possède une résistance intrinsèque à cette molécule lourde.
C'est le moment « wow » de l'enquête scientifique. Comment une bactérie confinée dans un trou noir géologique peut-elle posséder une clé qui ouvre la serrure de l'un de nos antibiotiques les plus sophistiqués ? La réponse réside dans le fait que LC231 produit probablement elle-même des composés similaires à la daptomycine pour éliminer ses concurrentes dans la grotte. Pour ne pas s'empoisonner elle-même, elle a dû évoluer pour devenir immunisée à sa propre arme. Ainsi, quand nous utilisons la daptomycine, LC231 la reconnaît comme une menace familière qu'elle sait déjà neutraliser depuis des millénaires. ! Détail microscopique de cellules bactériennes agrégées.
L'énigme de Lechuguilla : comment vaincre un médicament qu'on n'a jamais rencontré ?
La découverte de la grotte de Lechuguilla nous oblige à reconsidérer totalement notre définition des antibiotiques. Nous pensions avoir inventé ces molécules magiques au XXe siècle, mais la réalité est différente : nous avons seulement fait du « bio-prospecting ». Nous avons puisé dans l'arsenal chimique que la nature avait mis des millions d'années à concevoir. La résistance aux antibiotiques n'est donc pas une réponse à l'homme, mais une réponse à la guerre éternelle que les microbes se livrent entre eux dans le sol, l'eau et les profondeurs de la Terre.
Cette prise de conscience a été théorisée par Gerry Wright, un chercheur de l'Université McMaster, dès 2006. Il a démontré que les bactéries du sol ordinaire regorgent de gènes de résistance, bien avant que l'homme ne commence à utiliser des médicaments. Les recherches récentes, publiées dans des revues comme Frontiers in Microbiology en 2024, confirment que les gènes de résistance aux antibiotiques (ARG) ont une longue histoire évolutive qui précède largement la médecine humaine. Lechuguilla n'est pas une anomalie ; c'est le témoin le plus pur de cette vérité.
Les antibiotiques existent depuis bien avant Alexander Fleming
L'histoire de la médecine raconte souvent qu'Alexander Fleming a découvert la pénicilline en 1928 grâce à un heureux hasard. Cependant, pour le monde microbien, la pénicilline et ses cousins chimiques existent depuis des centaines de millions d'années. Les bactéries du sol, notamment les Actinobactéries, produisent des composés antimicrobiens pour éliminer leurs concurrentes et sécuriser leur accès aux ressources nutritives. C'est une stratégie écologique classique : empoisonner le voisin pour prospérer.
Par conséquent, toutes les bactéries qui ont survécu dans cet environnement, comme celles de Lechuguilla, ont co-évolué avec ces toxines naturelles. C'est une course à l'armement constante : si une bactérie produit une molécule toxique, ses voisines doivent développer une résistance sous peine de disparaître. La molécule que Fleming a isolée n'était qu'une version synthétique d'une arme que les bactéries utilisaient déjà depuis des ères géologiques. La résistance que nous observons aujourd'hui dans nos hôpitaux est donc simplement le résultat du transfert de ces stratégies de défense ancestrales vers des pathogènes modernes.
La course à l'armement évolutive : Lechuguilla comme fossile vivant de cette guerre
La grotte de Lechuguilla agit comme un fossile vivant de cette guerre microbienne. En étant isolée du monde extérieur, elle a figé un instant de l'évolution biologique. La souche Paenibacillus LC231 porte en elle les cicatrices de billions de batailles microscopiques. Son génome contient des traces d'anciens conflits, des défenses élaborées contre des menaces qui n'existent peut-être plus ailleurs.
Gerry Wright souligne que la diversité de la résistance aux antibiotiques dans la nature « devrait inspirer l'humilité ». Cela nous rappelle que nous avons rejoint une guerre en cours, pensant pouvoir la gagner avec des armes que les belligérants avaient déjà appris à contrer. La résistance n'est pas une nouvelle mutation accidentelle causée par l'homme ; c'est un trait évolutif fondamental, une « armure » que les bactéries ont perfectionnée pendant que les dinosaures parcouraient encore la surface de la Terre.
Cinq mécanismes de défense inédits découverts dans l'armure de Paenibacillus
L'analyse détaillée du génome de Paenibacillus LC231, publiée dans la prestigieuse revue Nature Communications en 2016, a révélé des surprises encore plus grandes que la simple résistance aux médicaments connus. Les chercheurs ont identifié ce qu'ils appellent un « résistome » intrinsèque : une collection de 18 éléments de résistance chromosomique intégrés directement dans l'ADN de la bactérie. Contrairement à la résistance acquise par échange de plasmides (souvent observée dans les hôpitaux), ici, la résistance fait partie intégrante de l'identité de l'organisme.
Mais le plus vertigineux est que parmi ces éléments, cinq n'ont aucun homologue connu dans les bases de données génétiques mondiales. En d'autres termes, la nature a inventé des méthodes pour neutraliser les antibiotiques que nos scientifiques n'avaient jamais vues ni imaginées. De plus, trois mécanismes de défense distincts n'avaient jamais été impliqués auparavant dans la résistance aux antibiotiques. Cela signifie que les bactéries de Lechuguilla possèdent un manuel de stratégie militaire entièrement inédit.
Un résistome de 18 éléments : décrypter l'ADN d'une survivante
Le concept de « résistome » est crucial pour comprendre l'ampleur du défi auquel nous sommes confrontés. Il s'agit de l'ensemble complet des gènes de résistance aux antibiotiques présents dans un organisme ou dans un écosystème donné. Chez Paenibacillus LC231, ce résistome est composé de 18 éléments chromosomiques, ce qui suggère une accumulation progressive de défenses sur une très longue période.
Ce n'est pas une adaptation rapide à une nouvelle menace, mais le résultat de 4 millions d'années de sélection naturelle. Chaque gène correspond à une bataille gagnée dans le passé, une victoire contre une toxine produite par un voisin microbien. Ces gènes sont stabilisés dans le chromosome, ce qui signifie qu'ils sont transmis fidèlement à chaque génération. C'est une bibliothèque de survie, constituée lentement au fond de la grotte, loin de toute influence humaine directe, mais terriblement pertinente pour nos problèmes médicaux actuels. ! Un scientifique tenant des solutions en laboratoire devant du matériel technique.

Cinq voies de résistance sans équivalent : un catalogue potentiel pour la médecine
L'identification de cinq déterminants de résistance sans équivalent connu est une découverte à double tranchant. D'un côté, elle est effrayante : elle prouve que la nature a en réserve des méthodes pour neutraliser nos médicaments que nous ne connaissons pas encore et contre lesquelles nous sommes totalement désarmés. Si ces gènes venaient à se transférer à des bactéries pathogènes, ils pourraient rendre inefficaces des classes entières d'antibiotiques que nous pensions sûrs.
D'un autre côté, ces mécanismes sont décrits par les chercheurs comme étant d'« intérêt clinique potentiel ». En comprenant comment LC231 parvient à détruire ou à expulser ces molécules, les scientifiques espèrent pouvoir inspirer de nouvelles pistes thérapeutiques. Il est possible de modifier nos antibiotiques existants pour contourner ces défenses, ou d'utiliser ces mécanismes comme cibles pour de nouveaux médicaments. La grotte, loin d'être seulement une menace, est aussi un réservoir de connaissances biologiques inestimable pour concevoir les médicaments du futur.
Le transfert horizontal de gènes : la piste qui relie Lechuguilla à nos hôpitaux
La question qui hante alors les microbiologistes est la suivante : si Paenibacillus LC231 n'est pas pathogène, quel est le risque réel pour l'homme ? La réponse réside dans un phénomène biologique fascinant appelé le transfert horizontal de gènes (HGT). Contrairement à la reproduction verticale, où un parent transmet ses gènes à sa descendance, le HGT permet aux bactéries d'échanger du matériel génétique entre elles, même si elles sont d'espèces différentes.
Imaginez des bactéries comme des ordinateurs connectés sur un même réseau, capables de s'envoyer des fichiers « piratés » contenant des codes pour déjouer les défenses. Une bactérie inoffensive dans une grotte pourrait théoriquement transférer ses gènes de résistance à une bactérie pathogène si elles venaient à se rencontrer. L'Institut Pasteur, notamment via son unité EMAE (Épidémiologie et Modélisation de l'Évasion Antibactérienne), étudie précisément comment ces échanges se produisent entre les microbiomes environnementaux et les pathogènes humains.
Quand les bactéries échangent leur ADN comme des fichiers piratés
Le transfert horizontal de gènes est un pilier de l'évolution bactérienne. Il peut se produire de plusieurs manières : la conjugaison (contact direct et échange d'ADN via un pont), la transformation (absorption d'ADN libre dans l'environnement) ou la transduction (transport par un virus bactériophage). Ces mécanismes permettent aux traits de résistance de se propager à une vitesse fulgurante à travers les populations microbiennes, agissant comme un réseau mondial de partage de données.
C'est ce processus qui rend la situation critique dans nos hôpitaux. Une bactérie environnementale, comme LC231, peut servir de réservoir silencieux de gènes de résistance. Si un pathogène vient à « télécharger » ce gène, il acquiert instantanément une superpuissance défensive sans avoir à attendre des millénaires d'évolution. C'est comme si une armée volait instantanément les plans d'un bouclier high-tech développé par une civilisation alien isolée. Bien que Lechuguilla soit scellée et que le risque direct soit faible, le même processus se produit quotidiennement dans nos sols, nos eaux usées et nos propres intestins.
Ce que l'Institut Pasteur dit du risque de dissémination
Les travaux menés à l'Institut Pasteur soulignent que les microbiomes environnementaux jouent un rôle pivot dans la dissémination de la résistance antibactérienne. Les chercheurs de l'unité EMAE modélisent comment ces gènes « envahissent » les populations pathogènes. Le cas de Lechuguilla, bien qu'extrême, sert de modèle parfait pour comprendre la dynamique de ces échanges.
Le risque n'est pas que la bactérie de la grotte sorte de son trou pour nous infecter. Le risque est que les mécanismes génétiques qu'elle porte, ou d'autres similaires présents dans l'environnement, finissent par se retrouver dans des bactéries que nous côtoyons quotidiennement. Les sols agricoles saturés d'antibiotiques, les eaux contaminées par les effluents hospitaliers ou même notre propre flore intestinale sont des lieux où ce « marché noir génétique » est très actif. Lechuguilla nous montre simplement que le potentiel de résistance est partout, prêt à être mobilisé.
1,14 million de morts par an : ce que les profondeurs nous disent de notre fragilité
Cette plongée dans les profondeurs de Lechuguilla n'est pas un exercice de curiosité scientifique abstraite. Elle nous ramène à une réalité brûlante : la crise mondiale de la résistance aux antimicrobiens (RAM). Selon les données les plus récentes de l'Organisation mondiale de la Santé (OMS) et des rapports cités par la BBC, la résistance aux antimicrobiens était directement responsable de 1,14 million de décès en 2021. Les estimations prévoient que 39 millions de personnes pourraient mourir à cause de la RAM entre 2025 et 2050 si aucune action majeure n'est prise.
La grotte de Lechuguilla nous offre une perspective cruciale pour comprendre cette catastrophe. Elle nous montre que nous ne combattons pas un ennemi que nous avons créé, mais une force fondamentale de la nature que nous avons imprudemment réveillée et accélérée. En utilisant des milliards de tonnes d'antibiotiques dans l'agriculture et la médecine, nous avons exercé une pression sélective titanesque sur les bactéries, favorisant la propagation des gènes de résistance qui dormaient depuis des millions d'années.
La résistance aux antimicrobiens : la pandémie silencieuse qui tue déjà 1,14 million de personnes chaque année
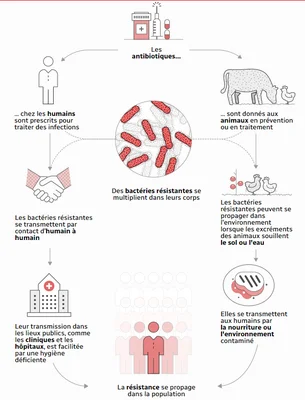
Les chiffres de l'OMS sont glaçants. La résistance aux antimicrobiens est décrite comme une « pandémie silencieuse ». Contrairement au COVID-19, qui a émergé soudainement, la RAM progresse lentement, inlassablement, dans l'ombre. Des infections banales, comme une coupure infectée ou une pneumonie, redeviennent mortelles car nos médicaments ne fonctionnent plus. Des millions d'enfants meurent chaque année de septicémies résistantes que nous aurions pu traiter il y a seulement vingt ans. ! Cycle de propagation des bactéries résistantes aux antibiotiques.
L'étude des bactéries de Lechuguilla nous apprend que ces agents pathogènes ne partent pas de zéro. Ils puisent dans un héritage génétique colossal. La bactérie LC231 n'est pas la cause de la crise, mais c'est le témoin à charge qui démontre l'immensité du réservoir de résistance naturel. Nous avons perdu la course à l'armement évolutive avant même de comprendre que nous y participions.
Lechuguilla, miroir de notre impasse : nous n'avons pas inventé la résistance, nous l'avons accélérée
La leçon ultime de la grotte de Lechuguilla est une leçon de modestie. Comme le souligne Gerry Wright, nous devons comprendre que l'utilisation des antibiotiques et la résistance vont de pair. En pensant que la découverte de la pénicilline nous donnait une domination totale sur les microbes, nous avons agi avec arrogance. Nous avons inondé la planète de nos dérivés synthétiques, croyant que la nature ne pouvait pas répondre aussi vite.
Mais la nature avait déjà la réponse. Lechuguilla est le miroir de notre impasse : nous avons accéléré un processus naturel qui s'étend sur des millions d'années, le compressant en quelques décennies. La résistance n'est pas une anomalie moderne ; c'est une caractéristique intrinsèque du vivant. Face à cette évidence, la seule stratégie viable n'est pas de chercher une « balle argentée » miracle, mais de repenser notre relation avec le monde microbien, en limitant l'usage de ces armes précieuses et en respectant l'équilibre fragile des écosystèmes qui nous entourent.
Sous nos pieds, une leçon de modestie microbienne
L'histoire de Paenibacillus LC231 et de la grotte de Lechuguilla est une parabole scientifique poignante. Au fond de ce labyrinthe scellé, à 400 mètres sous terre, vit une bactérie inoffensive pour l'homme mais terrifiante pour nos médicaments. Elle a survécu 4 millions d'années en développant des défenses que nous ne comprenons pas encore, défiant notre hubris technologique. Elle nous rappelle que nos « miracles » pharmaceutiques ne sont que des outils empruntés à un monde vivant infiniment plus ancien et plus ingénieux que nous.
La véritable leçon de Lechuguilla n'est pas la peur panique d'une épidémie venue des profondeurs, mais l'acceptation d'une réalité : nous ne sommes pas les maîtres de la biologie, mais ses utilisateurs temporaires. La crise des antimicrobiens ne se résoudra pas seulement par la découverte de nouvelles molécules, car la nature a déjà une longueur d'avance. Elle se résoudra peut-être en apprenant à comprendre, respecter et protéger ces écosystèmes anciens, tout en adaptant notre usage des antibiotiques pour ne plus déranger l'équilibre de cette guerre microbienne qui se déroule depuis des temps immémoriaux. Sous nos pieds, dans le silence de la roche, les bactéries nous murmurent une vérité simple : la vie trouve toujours un chemin.