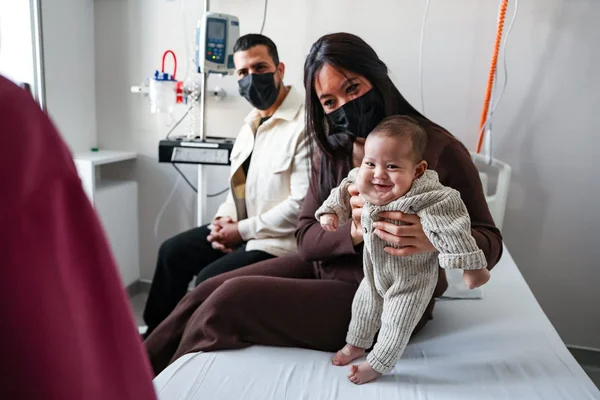
En décembre 2025, dans le silence respectueux du Queen Charlotte's and Chelsea Hospital de Londres, l'impossible s'est matérialisé sous la forme d'un cri nouveau-né. Hugo Powell voyait le jour, pesant 3,09 kg, un petit garçon dont l'existence redéfinit les limites de la biologie humaine. Il est le tout premier enfant né au Royaume-Uni grâce à une greffe d'utérus réalisée à partir d'une donneuse décédée. Si l'annonce officielle n'a été faite que deux mois plus tard, en février 2026, c'était pour laisser à la famille le temps de savourer ce miracle intime loin des feux de la rampe. Derrière ce prénom se cache le parcours héroïque de Grace Bell, sa mère, et d'une équipe médicale britannique qui a osé briser un tabou scientifique. C'est l'histoire d'une quête de maternité contre vents et marées, où une absence anatomique a été comblée par la solidarité d'une inconnue et la virtuosité de la chirurgie.
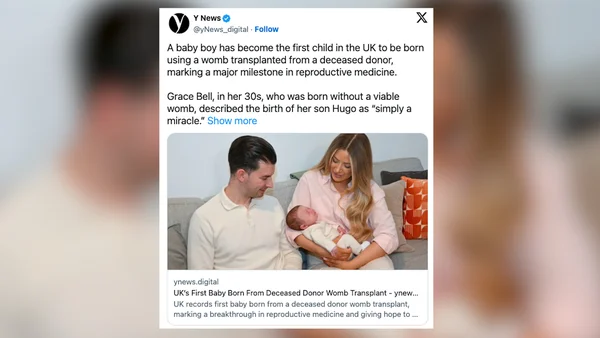
Hugo, 3,09 kg de vie après 14 ans d'attente
L'arrivée d'Hugo ne marque pas seulement une naissance, elle clôture quatorze années de combat médical et psychologique pour Grace Bell. À l'âge de 16 ans, le monde de cette jeune femme s'est effondré lorsqu'on lui a diagnostiqué le syndrome de Mayer-Rokitansky-Küster-Hauser (MRKH). Cette malformation congénitale rare se caractérise par l'absence ou le sous-développement de l'utérus et du vagin, bien que les ovaires fonctionnent parfaitement. L'annonce brutale d'une infertilité irréversible à l'aube de l'âge adulte laisse des traces profondes, transformant ce qui devrait être une évidence biologique en un horizon inaccessible.
De l'annonce dévastatrice à l'inimaginable
Le cheminement de Grace Bell est celui d'une résilience face à l'adversité. Pendant des années, la perspective de ne jamais porter d'enfant a été une source de douleur sourde. Pourtant, grâce à la détermination des équipes du NHS Blood and Transplant et aux avancées de la science reproductive, ce scénario a été bouleversé. Lorsqu'elle a tenu son fils pour la première fois, Grace a exprimé avec une simplicité désarmante l'ampleur de ce qui venait d'accomplir : « Depuis mes 16 ans, je n'aurais jamais imaginé que cela puisse se réaliser. C'est un véritable miracle. » Cette phrase résume le passage de l'abîme à la lumière, une transition rendue possible par un exploit chirurgical majeur.
Un accouchement sous haute surveillance à Londres
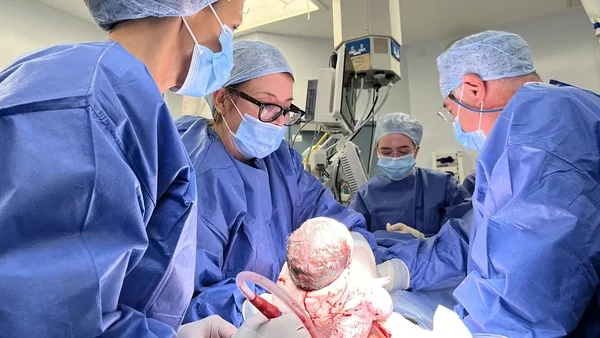
La naissance d'Hugo s'est déroulée dans des conditions de sécurité maximales. L'équipe médicale a opté pour une césarienne programmée, une procédure de rigueur dans ce contexte précis. En effet, un utérus greffé ne présente pas la même élasticité ni la même résistance aux contractions qu'un utérus naturel ; le risque de rupture utérine ou de complications hémorragiques durant l'accouchement par voie basse est trop élevé. L'intervention s'est déroulée au Queen Charlotte's and Chelsea Hospital, une institution référente en obstétrique. Le choix de ne rien publier avant février 2026 souligne le caractère pionnier et expérimental du protocole : il s'agissait d'abord de s'assurer de la stabilité de la mère et de l'enfant avant de briser la nouvelle, une prudence qui honore l'éthique médicale.
Syndrome MRKH : 1 femme sur 5000 privée d'utérus
Pour comprendre la portée de cet événement, il faut s'intéresser de près à la pathologie qui a motivé cette greffe. Le syndrome de Mayer-Rokitansky-Küster-Hauser (MRKH) n'est pas seulement une anomalie rare, c'est une spécificité anatomique qui touche environ une femme sur 5 000. Au Royaume-Uni, cela représente des milliers de femmes qui découvrent souvent à l'adolescence, lors de l'absence de premières règles, qu'elles ne pourront pas mener une grossesse naturellement. C'est une condition isolante qui touche à l'identité féminine et au projet de vie de nombreuses patientes.
Quand les ovaires fonctionnent mais l'utérus manque
La biologie du syndrome MRKH est d'une cruauté paradoxale. Les femmes qui en sont atteintes possèdent des ovaires parfaitement fonctionnels, produisent des ovules viables et ont un profil hormonal normal. En théorie, tout le « carburant » nécessaire à la création d'un enfant est présent. L'obstacle est purement structurel : l'absence de cavité utérine empêche l'implantation de l'embryon. C'est comme disposer d'une semence précieuse sans avoir de terre pour la semer. La fécondation in vitro est donc possible, mais sans utérus, la gestation reste impossible. La greffe d'utérus devient alors la seule porte d'entrée vers une grossesse biologique, transformant une stérilité anatomique en une condition traitable.
Pourquoi ni la GPA ni l'adoption ne suffisaient
Face à l'infertilité, des alternatives comme la gestation pour autrui (GPA) ou l'adoption existent. Cependant, pour de nombreuses femmes atteintes du MRKH, ces options ne répondent pas à l'envie profonde de vivre la grossesse. Le désir de Grace Bell n'était pas seulement d'avoir un enfant, mais de le porter, de ressentir les mouvements fœtaux et de vivre les transformations physiologiques de la maternité. De plus, la GPA est illégale à but lucratif au Royaume-Uni et complexe à encadrer, tandis que l'adoption est un parcours administratif et psychologique distinct de la filiation génétique. La greffe d'utérus apparaît donc comme une réponse technique à un besoin physiologique et émotionnel spécifique : celui de la maternité vécue de l'intérieur. Existe-t-on encore après avoir eu un enfant ?, se demandent souvent les nouvelles mères ; pour Grace, c'était l'étape cruciale de l'accouchement qui validait son statut de mère.
7 heures sous bistouri : l'exploit chirurgical d'Oxford
Si la naissance d'Hugo est l'aboutissement émotionnel, tout a commencé en réalité en juin 2024 au Churchill Hospital d'Oxford. C'est là que s'est joué le pari médical le plus audacieux : implanter un utérus complexe et richement vascularisé dans le corps de Grace Bell. Cette intervention a représenté un défi technique majeur, nécessitant une coordination chirurgicale d'une précision millimétrée. L'équipe a dû jongler avec des vaisseaux sanguins minuscules et des ligaments délicats pour créer un environnement viable pour une future grossesse.
Juin 2024 : une transplantation de 10 heures qui a failli échouer
Les chiffres de cette opération donnent le vertige. L'intervention complète s'est étalée sur dix heures au total, dont « juste moins de 7 heures » pour la transplantation proprement dite de l'organe. Durant ces heures, les chirurgiens ont dû reconnecter artères et veines pour assurer une vascularisation immédiate de l'utérus. Le moindre retard ou la moindre erreur de suture pouvait compromettre l'intégrité de l'organe. Selon le rapport détaillé publié par NHS Blood and Transplant, il y a eu des moments critiques, notamment sur la connexion vasculaire, qui auraient pu faire capoter le projet. La réussite finale, validée par la coloration rosée de l'utérus une fois le sang rétabli, est un triomphe de la microchirurgie.
FIV, transfert d'embryon et grossesse à risques
La greffe n'était que la première marche d'un escalier périlleux. Après une période de récupération, Grace Bell a dû suivre un protocole strict de fécondation in vitro à la Lister Fertility Clinic de Londres. Ses ovules avaient été prélevés avant l'opération, fécondés avec les spermatozoïdes de son partenaire Steve, et congelés. Le transfert de l'embryon dans l'utérus greffé a été un moment de tension extrême : allait-il s'implanter ? La grossesse qui a suivi a été classée à haut risque. Grace a dû prendre quotidiennement des immunosuppresseurs pour empêcher son corps de rejeter l'organe étranger, ce qui implique une surveillance médicale hebdomadaire pour équilibrer le risque de rejet et la santé du fœtus.
Pourquoi l'utérus sera retiré après la grossesse
Il est essentiel de noter que cette greffe n'est pas destinée à être définitive. Contrairement au cœur ou aux reins, l'utérus n'est pas un organe vital. Sa présence n'est nécessaire que le temps de mener une ou deux grossesses à terme. Le retirer après la maternité permet d'arrêter le traitement immunosuppresseur, qui sur le long terme augmente les risques d'infections, de cancers et de problèmes rénaux. C'est ce qu'on appelle une greffe « pont » : elle sert de véhicule vers la parentalité avant d'être retirée, laissant la mère vivre sa vie sans la lourdeur des médicaments anti-rejet. C'est une approche pragmatique qui privilégie la santé globale de la patiente sur le long terme.
L'utérus d'une inconnue décédée : le consentement qui change tout
L'un des aspects les plus poignants de cette histoire réside dans l'origine de l'organe. L'utérus qui a porté Hugo provenait d'une donneuse décédée, une femme dont l'identité reste anonyme mais dont le geste change la vie des Powell. Ce type de transplantation apporte une dimension symbolique forte, car il ne s'agit pas seulement d'un transfert biologique, mais d'un legs de vie à la postérité. Ce lien invisible entre une famille endeuillée et une famille en devenir touche au cœur de l'éthique du don.
Pourquoi le registre standard des donneurs ne suffit pas
Il est crucial de comprendre que la donation d'utérus n'est pas couverte par le registre standard des donneurs d'organes du Royaume-Uni, ni par le système de consentement présumé. Même si une personne a signifié sa volonté de donner ses organes de son vivant, l'utérus nécessite un consentement spécifique et supplémentaire de la famille après le décès. En effet, la greffe d'utérus est encore considérée comme expérimentale et n'est pas vitale pour la receveuse. Les équipes de coordination doivent donc aborder les familles avec une délicatesse extrême pour expliquer la spécificité de ce don et obtenir leur accord explicite. C'est une démarche qui demande beaucoup de tact, surtout dans le contexte du deuil immédiat.
Les mots des parents de la donneuse : « Son dernier choix fut un acte de pure générosité »
Dans le communiqué publié par l'hôpital, relayé par plusieurs médias dont Le Parisien, les parents de la donneuse ont partagé un témoignage bouleversant. Ils ont déclaré : « La perte de notre fille a bouleversé notre monde d'une manière que nous avons du mal à exprimer avec des mots […] nous avons cependant trouvé du réconfort dans le fait de savoir que son dernier choix fut un acte de pure générosité. » Ces mots illustrent la capacité de l'acte du don à transformer une tragédie en un héritage de vie. Pour Grace et Steve Powell, savoir que leur fils a pu voir le jour grâce à cet ultime sacrifice crée une dette de reconnaissance éternelle envers cette famille inconnue.
150 greffes dans le monde : le Royaume-Uni rejoint le club restreint
La naissance d'Hugo propulse le Royaume-Uni dans une catégorie très restreinte de nations pionnières en matière de reproduction. Cependant, il ne s'agit pas d'une découverte isolée, mais plutôt de l'aboutissement d'une décennie de recherches menées à l'échelle internationale. En examinant les statistiques mondiales, on mesure à quel point cette technologie est restée marginale, réservée à quelques centres d'excellence capables de surmonter les défis chirurgicaux et immunologiques qu'elle pose.
Suède 2014, Brésil 2017 : les pionniers de la greffe d'utérus
L'histoire moderne de la greffe d'utérus débute en Suède en 2014, où l'équipe du professeur Mats Brännström a annoncé la première naissance mondiale suite à une greffe réalisée à partir d'une donneuse vivante. Cette avancée majeure a prouvé la viabilité du concept, bien qu'elle impliquât des risques chirurgicaux pour la donneuse (souvent une proche de la receveuse). En 2017, le Brésil a franchi une nouvelle étape en réussissant la première naissance issue d'une donneuse décédée à l'hôpital das Clínicas de São Paulo. Cette étape était cruciale car elle validait un modèle éthique plus acceptable, ne mettant pas en danger la santé d'une femme vivante pour aider une autre.
Donneuse vivante ou décédée : deux tiers contre un tiers
À l'échelle planétaire, on recense environ 150 greffes d'utérus effectuées à ce jour, ayant permis la naissance de plus de 70 bébés en bonne santé. La répartition des sources des organes est néanmoins déséquilibrée : plus des deux tiers des greffes impliquent des donneuses vivantes, tandis qu'environ un tiers proviennent de donneuses décédées. Cela représente environ 25 à 30 bébés nés grâce à des donneuses décédées. La prédominance des donneuses vivantes s'explique par des raisons techniques : un organe prélevé sur une personne vivante souffre moins d'ischémie (manque d'oxygène) et la compatibilité immunologique est souvent meilleure. Cependant, l'évolution des protocoles tend à favoriser le modèle de la donneuse décédée pour éviter les risques pour les donneuses vivantes.
Coût et accessibilité : 30 000 livres par greffe
Une telle excellence médicale a un coût financier élevé. Chaque greffe d'utérus coûte environ 30 000 livres sterling. Cette somme couvre l'opération complexe, l'hospitalisation, la FIV et le suivi rigoureux sur plusieurs années. Au Royaume-Uni, ce coût n'est pas pris en charge par le NHS, mais financé par une association caritative spécifique, Womb Transplant UK. Ce modèle de financement privé soulève des questions d'équité : l'accès à cette technique sera-t-il réservé à celles qui peuvent lever des fonds ou à celles vivant dans des pays riches ? Alors que la technique se mature, le débat sur sa prise en charge par les systèmes de santé publics devient incontournable pour éviter une médecine à deux vitesses en matière de fertilité.
Et en France ? Le projet de Rennes face aux freins bioéthiques
Alors que le Royaume-Uni célèbre son succès, la France n'est pas en reste mais avance avec une prudence législative caractéristique. L'Hexagone dispose d'une expertise médicale de premier plan, notamment à travers le CHU de Rennes, qui tente de lancer son propre protocole de greffe d'utérus. Cependant, ce projet se heurte à un cadre bioéthique strict et à des questions éthiques complexes qui ralentissent son aboutissement clinique comparé à ses voisins européens.
Le protocole de Rennes : 16 transplantations prévues mais aucun bébé encore
Le projet français est ambitieux et structuré autour d'un protocole financé par le Programme Hospitalier de Recherche Clinique (PHRC). L'objectif est de réaliser seize transplantations : huit issues de donneuses vivantes et huit de donneuses en état de mort cérébrale. Ce plan mixte vise à comparer les deux approches. Cependant, la supervision est draconienne. L'Agence nationale de sécurité du médicament (ANSM), l'Agence de la biomédecine et un comité de surveillance indépendant scrutent chaque étape. À ce jour, aucun bébé n'est encore né de ces greffes en France, ce qui contraste avec l'accélération observée à l'étranger. La France privilégie une validation scientifique lente et incontestable avant d'envisager une généralisation.
Loi de bioéthique 2021 : ce qui a changé et ce qui reste interdit
La loi de bioéthique révisée en 2021 a marqué des progrès significatifs en matière de droits reproductifs en France, notamment l'ouverture de l'assistance médicale à la procréation (AMP) aux couples de femmes et aux femmes célibataires, ainsi que l'autorisation des « dons combinés ». Néanmoins, la greffe d'utérus reste classée comme une « recherche clinique » et non comme un soin de routine. Cela signifie qu'elle n'est pas interdite, mais qu'elle ne peut se pratiquer que dans le cadre d'essais thérapeutiques très encadrés. Contrairement à d'autres pays où la demande patiente peut parfois presser la législation, la France maintient une distinction claire entre innovation et soin standard.
Quand l'éthique française refuse l'obstination déraisonnable
Un cas spécifique étudié par les chercheurs du projet Rennes illustre les dilemmes éthiques français. Il concerne une patiente de 32 ans atteinte du MRKH, en couple avec une femme possédant un utérus fonctionnel. Théoriquement, la partenaire aurait pu porter l'enfant, mais elle a refusé. Le comité d'éthique a dû déterminer si la greffe d'utérus était justifiée malgré cette alternative biologique existante. Finalement, le comité a validé la participation de la patiente, jugeant que le désir de vivre soi-même la grossesse était un besoin légitime qui ne devait pas être sacrifié simplement parce qu'une autre solution existait pour le couple. Ce débat montre que l'éthique française cherche un équilibre subtil entre évitement de l'obstination déraisonnable et respect du projet de vie personnel.
Demain, un utérus pour tous ? Les frontières que la médecine s'apprête à franchir
Avec la réussite de Hugo et l'accumulation des connaissances, la communauté scientifique commence à regarder vers l'avenir et à s'interroger sur les limites de cette technologie. Aujourd'hui réservée aux femmes nées sans utérus ou ayant subi une hystérectomie, la greffe d'utérus pourrait théoriquement s'étendre à d'autres catégories de population. Ces perspectives ouvrent des horizons vertigineux, mais soulèvent également des questions éthiques et sociétales majeures qui n'attendent que d'être posées.
Femmes transgenres, hommes cisgenres : jusqu'où ira la transplantation ?
La possibilité d'étendre la greffe d'utérus aux femmes transgenres est un sujet de débat scientifique croissant. Bien que les défis techniques soient immenses — nécessitant une reconstruction du canal pelvien et une connexion nerveuse complexe — certains chercheurs y voient une prochaine frontière logique. Pour les hommes cisgenres, l'obstacle semble encore plus infranchissable, impliquant des modifications structurelles du squelette et une gestion hormonale extrême. Si ces scénarios restent pour l'heure spéculatifs, l'histoire de la médecine montre que l'impossible d'aujourd'hui peut devenir la réalité de demain. Cela nous force à nous demander : la grossesse est-elle intrinsèquement liée au sexe biologique féminin tel que nous le connaissons, ou peut-elle devenir une option ouverte à tous ceux qui la désirent ?
Alternative à la GPA ou nouvelle marchandisation du corps ?
La greffe d'utérus est souvent présentée comme l'alternative éthique ultime à la gestation pour autrui (GPA). Elle permettrait en effet à une femme de porter son enfant sans avoir recours au corps d'une tierce personne, évitant ainsi les risques d'exploitation économique liés à la GPA commerciale. C'est l'argument du « ventre propre » et autonome. Cependant, une critique émergente suggère que la greffe pourrait participer à une autre forme de marchandisation. Avec des coûts avoisinant les 30 000 livres et dépendance potentielle à des donneuses, ne risque-t-on pas de créer un marché de l'utérus où seuls les plus riches pourront s'offrir le luxe de porter un enfant biologique ? La frontière entre progrès médical et technologie de luxe reproductive devient ténue, appelant à une vigilance législative forte.
Conclusion : Hugo, symbole d'une nouvelle ère reproductive
La naissance d'Hugo Powell marque un tournant décisif dans l'histoire de la médecine reproductive. Elle valide le concept selon lequel l'utérus n'est plus une fatalité biologique, mais un organe remplaçable capable de créer la vie. Pour les milliers de femmes atteintes du syndrome MRKH ou ayant perdu leur utérus, cette avancée offre un souffle d'espoir inédit, là où il n'y avait que le silence. Elle prouve que la persévérance scientifique, couplée à la générosité du don d'organes, peut repousser les barrières de l'infertilité absolue.
Cependant, ce miracle médical s'accompagne de responsabilités. Les questions éthiques concernant l'accessibilité financière, l'origine des organes et les limites de la technologie doivent être débattues au grand jour. Alors que la France continue d'avancer avec prudence à Rennes et que le Royaume-Uni ouvre la voie, le monde doit réfléchir à l'encadrement de ces nouveaux pouvoirs. Hugo est le premier d'une nouvelle lignée d'enfants nés de la science et de la solidarité ; à nous de veiller à ce que cette ère reproductive reste au service de l'humanité et de l'équité.