Dans le monde de la régulation pharmaceutique, réputé pour sa lenteur et sa prudence, un événement sismique vient de bouleverser les codes. Le 1er avril 2026, l'agence américaine des produits alimentaires et médicamenteux (FDA) accordait son feu vert à Foundayo, le nouveau traitement contre l'obésité du laboratoire Eli Lilly. Ce qui stupéfie pourtant les observateurs n'est pas tant l'efficacité de la molécule que la vitesse fulgurante de son processus de validation : cinquante jours à peine. En comparaison, une procédure classique d'examen d'un nouveau médicament s'éternise généralement entre dix et douze mois. Comment une institution célèbre pour sa lourdeur bureaucratique a-t-elle pu pulvériser ses propres standards chronométriques ? Cette précipitation inédite cache-t-elle un revirement stratégique majeur dans la gestion des crises de santé publique ? Plongeons au cœur de cette anomalie administrative et scientifique.
L'anomalie des cinquante jours : une procédure express qui pulvérise les standards
Pour saisir l'ampleur du phénomène, il faut visualiser l'habituel parcours du combattant d'un médicament. Typiquement, l'examen d'une Nouvelle Entité Moléculaire s'apparente à un marathon de plusieurs mois, durant lequel l'agence scrute chaque donnée clinique, chaque effet secondaire potentiel et chaque détail de fabrication avec une loupe minutieuse. C'est un processus nécessaire, visant à garantir que les bénéfices l'emportent nettement sur les risques. Avec Foundayo, ce marathon a soudainement été couru au rythme d'un sprint de 100 mètres. Selon les déclarations de la FDA et du laboratoire Eli Lilly, l'analyse du dossier a été bouclée en cinquante jours, ce qui en fait l'approbation la plus rapide d'une molécule totalement inédite depuis 2002.
Cette accélération brutale interroge sur la nature même du contrôle exercé par l'État. Loin d'être un hasard, cette rapidité est le résultat direct d'une refonte politique des priorités de santé, opérée sous pression économique et sanitaire. L'obésité n'est plus seulement considérée comme un problème de santé individuel, mais comme une crise nationale pesant des milliards de dollars sur l'économie américaine. En conséquence, les freins administratifs habituels ont été desserrés, créant une tension fascinante entre l'impératif de mise à disposition rapide des traitements et la nécessité impérieuse de sécurité. Cette dynamique force à se demander si nous assistons à une « Uberisation » de l'accès aux soins, où la vitesse devient le premier critère de succès, reléguant parfois la prudence au second plan.
Cette décision survient dans un contexte particulier de turbulence au sein de la haute administration sanitaire, où les débats sur l'avenir de la régulation sont vifs. On se souvient que Vinay Prasad quitte la FDA et que son départ en avril 2026 a suscité de nombreuses interrogations sur l'indépendance de l'agence face aux géants de l'industrie pharmaceutique. C'est dans cet climat de transition que Foundayo a reçu son sésame, laissant penser que l'agence est en train de réécrire les règles du jeu en temps réel.
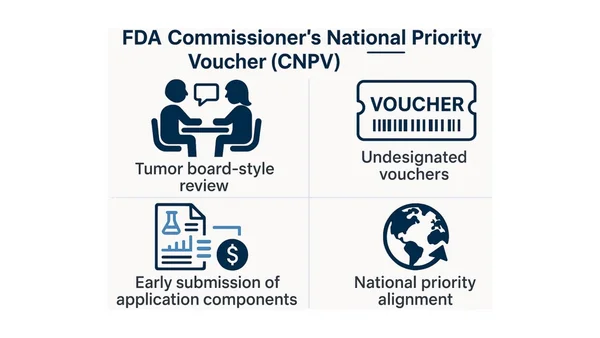
Le « Commissioner's National Priority Voucher » : le coupe-file inédit de 2025

Le secret de cette vitesse fulgurante réside dans un outil bureaucratique tout droit sorti d'une boîte à outils gouvernementale récemment débloquée. Intitulé le « Commissioner's National Priority Voucher » (CNPV), ce programme a été lancé en juin 2025 avec un objectif explicite : drastiquement réduire le temps de révision pour les médicaments jugés cruciaux pour la nation. Le principe est simple sur le papier mais révolutionnaire dans les faits : si un traitement est aligné sur des priorités nationales clairement définies, le temps d'examen passe d'une moyenne de dix à douze mois à une fourchette comprise entre un et deux mois.
C'est la première fois que l'on voit un tel mécanisme de coupe-file appliqué à si grande échelle pour une maladie chronique non infectieuse. Foundayo a ainsi bénéficié de ce statut privilégié, devenant le cinquième médicament à être approuvé sous ce régime. Cependant, il y a une nuance capitale : contrairement aux quatre précédents qui étaient souvent des dérivés ou des améliorations de thérapies existantes, Foundayo est la toute première « Nouvelle Entité Moléculaire » à passer par cette voie express. Cela signifie que la FDA a non seulement accéléré la procédure, mais l'a fait pour une substance chimique que l'organisme n'avait jamais vue auparavant.
Ce choix politique illustre une volonté manifeste de traiter l'obésité avec la même urgence que les épidémies virales ou les menaces biologiques. En utilisant le CNPV, les autorités américaines envoient un message clair : le temps de la patience réglementaire est révolu face à l'urgence de la situation sanitaire. C'est un pari audacieux qui consiste à miser sur la flexibilité administrative pour débloquer des solutions thérapeutiques majeures, espérant que les gains de santé publique surpasseront les risques inhérents à une revue plus rapide.
Le mystère temporel : 50 jours face au calendrier de référence
Si la communication officielle ne cesse de vanter ces cinquante jours, une plongée dans la chronologie exacte révèle une réalité plus nuancée, presque labyrinthique. Le chiffre autoproclamé de « 50 jours » correspond en réalité au temps de révision effectif, c'est-à-dire la période durant laquelle les scientifiques de la FDA ont activement travaillé sur le dossier une fois les formulaires administratifs complétés. Cependant, si l'on remonte le fil jusqu'à la soumission initiale du dossier par Eli Lilly, l'ensemble du processus s'étend sur une durée plus proche des cent jours, comme l'a souligné le magazine Time.
Cette distorsion s'explique par le jeu complexe des dates limites réglementaires, connues sous l'acronyme PDUFA (Prescription Drug User Fee Act). Initialement, la date limite butoir fixée par la FDA pour statuer sur Foundayo n'était pas prévue avant janvier 2027. En parvenant à une décision dès le début avril 2026, l'agence a non seulement respecté son délai de révision interne de cinquante jours, mais elle a également devancé son propre calendrier prévisionnel de plusieurs mois.

Cette différence entre le « temps d'horloge » et le « temps bureaucratique » est cruciale pour comprendre l'ampleur de l'accélération. D'un point de vue purement administratif, Eli Lilly a gagné près de neuf mois par rapport au calendrier standard. C'est un avantage commercial colossal dans un secteur où être le premier sur le marché se chiffre en milliards de dollars de recettes. Cela démontre que le programme CNPV ne se contente pas de hâter l'analyse scientifique ; il permet de court-circuiter les phases d'attente habituelles, transformant une procédure linéaire en un processus à haute vélocité.
Un contexte marqué par le doute scientifique
L'utilisation de ce mécanisme accéléré pour une molécule entièrement nouvelle ne s'est pas faite sans susciter de vives interrogations au sein de la communauté scientifique. L'approbation en cinquante jours d'une Nouvelle Entité Moléculaire impose une pression immense sur les équipes d'évaluation de la FDA. Habituellement, l'examen des données pharmacologiques, toxicologiques et cliniques s'effectue sur une durée permettant des aller-retours avec le laboratoire pour clarifier des points obscurs ou demander des analyses complémentaires.
Ici, la contrainte temporelle a forcément modifié la nature de l'examen. On peut légitimement se demander si tous les risques potentiels, notamment ceux liés à des effets secondaires rares ou tardifs, ont pu être écartés avec la certitude habituelle. La prudence de Tracy Beth Høeg, directrice par intérim du Centre d'évaluation et de recherche sur les médicaments (CDER), qui a mentionné une « analyse bénéfice-risque rigoureuse », masque peut-être une tension entre les exigences de sécurité et les pressions politiques pour une mise sur le marché rapide.
C'est toute la question de la balance bénéfices/risques qui se pose avec une acuité renouvelée. Si l'obésité représente indéniablement un risque de santé majeur, responsable de milliers de décès prématurés chaque année, l'introduction précipitée d'une nouvelle molécule chimique pourrait exposer la population à des risques jusqu'alors invisibles. Ce contexte de doute scientifique, loin d'être apaisé par l'annonce triomphale du laboratoire, pèse sur la perception de cette innovation thérapeutique.
Orforglipron : la chimie de la commodité derrière le comprimé Foundayo
Au-delà de la prouesse administrative, l'objet de toute cette effervescence mérite que l'on s'y attarde. Pourquoi ce médicament spécifique justifie-t-il un tel dérèglement des procédures ? La réponse réside dans la nature même de la molécule, l'orforglipron. Jusqu'à présent, les stars du traitement de l'obésité, comme l'Ozempic ou le Wegovy, souffraient d'une contrainte majeure : leur administration nécessite une injection sous-cutanée hebdomadaire. Or, l'observance d'un traitement à long terme est souvent le talon d'Achille de la médecine préventive. En transformant une injection contraignante en une simple pilule quotidienne, Eli Lilly n'a pas seulement amélioré un médicament, elle a changé la donne en matière d'acceptabilité sociale et personnelle du traitement.
C'est une avancée technologique majeure qui répond à une demande silencieuse mais massive des patients. Les injections, bien que devenues plus courantes, restent perçues comme une barrière, une pénalité corporelle infligée pour perdre du poids. La pilule, elle, s'inscrit dans la routine habituelle, celle des vitamines, du café matinal ou des médicaments contre la tension. En banalisant la prise du traitement, Foundayo promet d'industrialiser l'accès à la perte de poids, rendant la thérapie accessible à ceux qui refusent l'idée de s'injecter une substance à vie.
De l'aiguille à la gélule : le génie de la petite molécule

Pour comprendre la révolution, il faut faire un peu de chimie, mais rassurez-vous, c'est plus simple qu'il n'y paraît. Les traitements injectables actuels reposent sur des peptides. En termes simples, ce sont des chaînes d'acides aminés, un peu comme des perles enfilées. Le problème, c'est que notre estomac est conçu pour décomposer ces chaînes en nutriments. Si vous avalez un peptide comme celui de l'Ozempic, il est immédiatement détruit par les acides gastriques avant de pouvoir agir. C'est pour cela que l'injection est obligatoire : on contourne la barrière de l'estomac pour introduire le médicament directement dans le corps.
L'ingéniosité de Foundayo réside dans le fait que son principe actif, l'orforglipron, n'est pas un peptide. C'est ce que Daniel Skovronsky, le directeur scientifique d'Eli Lilly, appelle une « petite molécule chimique ». Découverte à l'origine par le laboratoire japonais Chugai Pharmaceutical, cette structure moléculaire est suffisamment robuste pour survivre au passage dans l'acide de l'estomac et assez petite pour traverser facilement la paroi intestinale pour passer dans le sang. Comme l'a expliqué Skovronsky, nous avons créé une molécule qui pénètre dans le corps plus facilement que les peptides injectés, tout en imitant leurs effets.
Cette distinction chimique est la clé de tout. Elle permet une administration orale sans restriction alimentaire : le médicament peut être pris à n'importe quelle heure, avec ou sans repas. Cette flexibilité contraste fortement avec la version orale de la concurrence, le Wegovy pilule, qui est encore un peptide modifié et qui exige d'être pris à jeun, avec une attente de trente minutes avant de manger. Avec Foundayo, la barrière biologique est tombée, rendant le traitement aussi simple que de prendre un paracétamol.

L'observance améliorée par la simplicité
L'un des défis majeurs dans le traitement des maladies chroniques est l'adhérence thérapeutique, ou la capacité du patient à suivre son traitement à la lettre sur le long terme. Les injections, bien qu'efficaces, posent souvent des problèmes d'acceptation : peur des aiguilles, douleur, rougeurs au site d'injection, ou simplement la contrainte de devoir se préparer une dose chaque semaine. Ces obstacles, parfois mineurs en apparence, se cumulent et finissent par entraîner un abandon du traitement pour une fraction significative de patients.
Le Dr Pouya Shafipour, spécialiste en médecine familiale et de l'obésité, souligne l'importance de ce changement de format. Selon lui, « c'est une étape importante d'avoir un autre comprimé de GLP-1 ». Il note que les gens sont habitués à prendre des pilules et que « se faire une piqûre toute sa vie n'est pas amusant ». En remplaçant l'injection par un geste aussi banal que celui d'avaler un comprimé, Foundayo maximise les chances que le patient reste fidèle à son traitement sur la durée nécessaire pour obtenir des résultats durables.

Cette facilité d'utilisation ne concerne pas seulement le confort immédiat, mais aussi la discrétion sociale. Une pilule peut se prendre n'importe où, au bureau ou au restaurant, sans attirer l'attention. Cette discrétion permet aux patients de gérer leur traitement sans avoir à justifier ou à expliquer leur démarche médicale à leur entourage, réduisant ainsi la charge psychologique souvent associée à la prise en charge de l'obésité.
Le compromis de l'efficacité : pas plus performant, mais plus accessible
Il est important de tempérer l'enthousiasme par une analyse lucide des données cliniques. Si l'accessibilité est en nette amélioration, l'efficacité brute de Foundayo ne surpasse pas miraculeusement celle des injections existantes. Les résultats des essais cliniques sont solides mais pas surnaturels : le groupe de patients ayant reçu la dose maximale a perdu en moyenne 12,4 kg sur 72 semaines, soit environ 12,4 % de leur poids corporel initial. C'est un résultat comparable à ce que l'on observe avec les injections, sans les dépasser de manière significative.
Dave Ricks, le PDG d'Eli Lilly, a d'ailleurs été très transparent à ce sujet lors de son passage sur CNBC. Il a souligné qu'il s'agissait d'un « grand moment », non pas parce que la pilule est plus puissante, mais parce qu'elle est « plus accessible, plus facile à intégrer dans votre routine quotidienne ». C'est une reconnaissance implicite que la bataille de l'obésité ne se gagnera pas seulement par la puissance pharmacologique, mais par la facilité d'utilisation.
Cependant, cette approche comporte un risque potentiel de banalisation. Si la pilule est perçue comme anodine parce qu'elle ressemble à n'importe quel autre médicament, on pourrait craindre une utilisation moins respectueuse des indications médicales. La facilité est un atout majeur pour l'observance, mais elle peut aussi devenir une tentation pour l'automédication ou la demande de prescriptions injustifiées. Le défi pour les médecins sera de maintenir un discours sérieux et encadré sur un produit qui, par sa forme même, invite à la légèreté.

Le grand écart transatlantique : l'attentisme de l'Europe face au feu vert américain
Cette validation express américaine crée un choc des cultures médicales assez brutal des deux côtés de l'Atlantique. Tandis que les États-Unis célèbrent l'innovation et la vitesse, l'Europe, et plus particulièrement la France, adopte une posture nettement plus frileuse. Cette divergence soulève des questions importantes sur l'équilibre entre innovation rapide et sécurité sanitaire à long terme. Pour un patient français ou européen, l'accès à Foundayo risque d'être beaucoup plus compliqué, encadré et différé que pour son homologue américain, créant une frustration potentielle compréhensible.
Cette différence d'approche n'est pas nouvelle, mais elle est exacerbée par l'utilisation du programme CNPV. L'Europe dispose de ses propres procédures d'accélération, mais elles sont rarement utilisées avec une telle radicalité pour des maladies chroniques non infectieuses. La prudence de l'Autorité européenne de sécurité des aliments (EFSA) et des agences nationales repose sur une philosophie de précaution qui peut sembler archaïque face à la dynamique américaine, mais qui assure souvent une meilleure traçabilité des effets secondaires à long terme.
Les critères stricts de l'ANSM : la fin de la prescription de confort
En France, le message est clair : l'obésité est une maladie grave qui doit être traitée comme telle, et non comme un souci esthétique. L'Agence nationale de sécurité du médicament et des produits de santé (ANSM) maintient une surveillance renforcée et continue sur tous les analogues du GLP-1, la classe de médicaments à laquelle appartient Foundayo. Contrairement à une approche libérale qui pourrait laisser chaque médecin décider, la France a verrouillé les conditions de prescription et de délivrance pour éviter tout glissement vers une médecine de convenance.
Ainsi, l'accès à ces traitements est strictement réservé aux patients présentant une obésité sévère, caractérisée par un indice de masse corporelle (IMC) supérieur à 35, ou à un IMC supérieur à 30 mais seulement s'il est accompagné de complications de santé majeures comme un diabète de type 2, de l'hypertension ou des troubles cardiovasculaires. Cette réglementation vise explicitement à empêcher que Foundayo ne devienne une « pilule minceur » utilisée par des personnes désirant perdre simplement quelques kilos pour l'été.
Pour les médecins français, cette approbation ultra-rapide aux États-Unis ne changera probablement rien à leur pratique immédiate. L'ANSM a fait évoluer les conditions de prescription précisément pour sécuriser l'utilisation de ces molécules puissantes. L'agence insiste sur le fait que ces médicaments ne doivent être prescrits qu'en complément d'un régime alimentaire dédié et d'une activité physique accrue. C'est une vision holistique de la santé qui refuse le raccourci d'une pilule miracle sans accompagnement, une vision qui pourrait sembler démodée aux yeux des partisans de l'innovation à tout va.
L'incertitude sur la disponibilité et le prix en Europe
Face à l'annonce triomphale d'Eli Lilly, le silence relatif des autorités sanitaires européennes est troublant. À l'heure actuelle, on ne dispose d'aucune information précise concernant le prix de Foundayo en Europe ni une date de commercialisation envisagée. Le laboratoire a proposé le médicament dans plus de 40 pays, mais il n'est pas certain qu'il y figure, du moins pas dans la première vague. Cette absence de visibilité laisse planer un doute sur la stratégie du laboratoire : va-t-il privilégier le marché américain, où la voie est libre, ou tenter une percée européenne face à une régulation plus exigeante ?
Cette attente risque de créer une frustration croissante chez les patients européens qui suivent de près les avancées outre-Atlantique. L'accès à l'information étant global, les Européens sont désormais conscients de l'existence de solutions potentielles, mais se heurtent aux murs de leur propre système de santé. Ce décalage temporel entre l'approbation américaine et la disponibilité européenne nourrit le débat sur l'harmonisation des normes sanitaires internationales et la capacité de l'Europe à suivre le rythme de l'innovation pharmaceutique.
En outre, l'absence de remboursement anticipé par la sécurité sociale constitue un autre frein majeur. Sans prise en charge par l'État, le coût du traitement, qui devrait s'aligner sur les prix très élevés des injections actuelles, le réservera de facto à une élite fortunée. C'est tout le paradoxe de cette industrialisation thérapeutique : elle promet d'aider le plus grand nombre, mais les contraintes économiques et réglementaires pourraient en restreindre l'accès, créant une société à deux vitesses en matière de santé métabolique.
La vigilance accrue face aux effets secondaires
L'un des arguments majeurs justifiant la prudence européenne concerne la sécurité à long terme. L'obésité étant une condition chronique, les traitements sont destinés à être pris sur des années, voire des décennies. Les études cliniques, même si elles sont étendues, ne permettent pas toujours de détecter des effets secondaires rares ou qui n'apparaissent qu'après une très longue exposition.
Le laboratoire Eli Lilly lui-même avertit que Foundayo peut provoquer des tumeurs de la thyroïde, y compris un cancer. Cette information, basée sur des études animales, figure en bonne place dans la notice et impose une surveillance rigoureuse. Les autorités sanitaires européennes sont particulièrement sensibles à ce type de risque. Elles préfèrent souvent attendre d'avoir un recul suffisant sur les populations traitées à grande échelle avant d'octroyer leur approbation définitive.
Cette différence de philosophie entre le « primum movere » américain (bouger vite) et le « primum non nocere » européen (d'abord ne pas nuire) risque de se cristalliser autour de Foundayo. L'Europe pourrait exiger des études post-commercialisation spécifiques ou des restrictions d'usage plus strictes, retardant d'autant plus la mise à disposition des patients. Il est fort à parier que le dossier de Foundayo va subir des examens particulièrement minutieux de la part de l'Agence européenne des médicaments (EMA), qui pourrait ne pas se satisfaire des seules garanties fournies par la FDA.
Guerre des laboratoires : l'offensive d'Eli Lilly contre l'empire Novo Nordisk
Il ne faut pas s'y tromper : derrière les aspects sanitaires et réglementaires, l'approbation de Foundayo est avant tout un coup de maître stratégique sur l'échiquier économique mondial. L'obésité est devenue le nouvel eldorado de l'industrie pharmaceutique, un marché évalué à des dizaines de milliards de dollars et en pleine expansion. Jusqu'à récemment, le danois Novo Nordisk régnait en maître quasi absolu avec son blockbuster Wegovy. Avec Foundayo, l'américain Eli Lilly ne se contente pas de proposer une alternative, il lance une offensive directe pour briser ce monopole et conquérir des parts de marché.
Cette rivalité entre les deux géants pharmaceutiques est comparable à une course à l'armement technologique. Chaque innovation de l'un est immédiatement contrée par une percée de l'autre. En validant Foundayo en un temps record, la FDA a peut-être aussi donné un avantage tactique précieux à Eli Lilly, lui permettant de prendre ses adversaires de vitesse et de saturer le marché avant même que la concurrence ne puisse réagir. C'est une guerre économique qui se joue avec la santé de millions de personnes comme enjeu, où la rapidité de mise sur le marché peut dicter le vainqueur.
La riposte orale au monopole du Wegovy
Depuis des mois, Novo Nordisk profitait d'une position dominante grâce à son double arsenal : l'injection Wegovy et, depuis décembre précédent, sa version orale. Ce monopole de fait sur la pilule anti-obésité était une aubaine pour le laboratoire danois, lui permettant de capturer les patients réticents aux injections. L'arrivée du Foundayo d'Eli Lilly change radicalement la donne en brisant cette exclusivité naissante.
Désormais, les médecins et les patients auront le choix entre deux molécules orales distinctes. Cette compétition est une excellente nouvelle pour le consommateur, car elle devrait théoriquement stimuler l'innovation et faire pression sur les prix. Les laboratoires ne pourront plus se reposer sur leurs lauriers ; ils devront prouver la supériorité ou au moins l'équivalence de leur produit pour convaincre la communauté médicale.
La réaction de Novo Nordisk n'a d'ailleurs pas tardé. Jamey Millar, vice-président exécutif des opérations américaines du groupe danois, a immédiatement contre-attaqué en affirmant que « tous les GLP-1 ne se valent pas ». Dans un communiqué virulent, l'entreprise a dénoncé comme trompeurs les rapports suggérant que l'orforglipron pourrait être plus efficace que la pilule Wegovy, soulignant qu'aucun essai comparatif direct n'avait encore été réalisé. C'est la preuve que la bataille ne se fait pas seulement dans les laboratoires de recherche, mais aussi sur le terrain de la communication et de la perception publique.
Une concurrence qui stimule l'innovation
Cette rivalité ne se limite pas à l'efficacité brute ou à la commodité de la pilule. Elle pousse les deux géants à explorer de nouvelles frontières thérapeutiques pour se différencier. Au-delà de la simple perte de poids, les recherches se portent désormais sur les bénéfices cardiovasculaires, la réduction des événements cardiaques majeurs ou l'amélioration de la santé rénale.
Les données des essais cliniques de Foundayo montrent d'ailleurs qu'il ne s'agit pas seulement de faire fondre la graisse. Le traitement a entraîné une réduction significative de nombreux marqueurs de risque cardiovasculaire, notamment le tour de taille, le cholestérol non-HDL, les triglycérides et la pression artérielle systolique. Eli Lilly peut donc arguer que sa pilule offre une protection métabolique globale, un argument de vente crucial face à des médecins soucieux de la santé globale de leurs patients.
Cette bataille de l'innovation profite in fine au patient. Elle force les laboratoires à investir massivement dans la recherche pour ne pas perdre pied. On peut s'attendre à voir apparaître, dans les années à venir, des générations de médicaments toujours plus performants, aux effets secondaires réduits et à l'efficacité accrue. Foundayo n'est peut-être qu'une étape dans une longue série d'avancées rendues possibles par cette compétition féroce entre deux des plus grandes entreprises pharmaceutiques au monde.
L'enjeu économique de la couverture maladie
Cependant, il existe un frein majeur qui pourrait limiter l'impact de cette guerre des prix : la couverture maladie. Comme le souligne justement NPR, même si la pilule est disponible et approuvée, son coût d'achat reste prohibitif pour la majorité de la population sans une prise en charge par l'assurance. Aux États-Unis, où les mutuelles de santé gèrent leur propre liste de médicaments remboursés, Foundayo va devoir se battre pour figurer sur les formules les plus courantes.
Si la pilule n'est pas remboursée ou reste trop onéreuse, l'accessibilité tant vantée par Eli Lilly restera théorique pour une large frange de la population. Les travailleurs précaires ou les classes moyennes, souvent les plus touchées par l'obésité, pourraient se retrouver exclus de cette révolution thérapeutique pour des raisons purement économiques. C'est le paradoxe amer d'un système qui inonde le marché de solutions médicales de pointe tout en laissant une partie significative des citoyens sur le bord de la route faute de moyens.
Eli Lilly va devoir naviguer entre deux écueils : fixer un prix qui récompense l'énorme investissement en recherche et développement, tout en restant suffisamment compétitif pour convaincre les assureurs et s'attirer la faveur des autorités publiques. Cette équation complexe déterminera si Foundayo sera un produit de niche réservé aux plus aisés ou un véritable levier de santé publique.
Effets secondaires et profil de tolérance : ce que les patients doivent savoir
Si l'arrivée de Foundayo est saluée comme une avancée majeure, elle ne doit pas faire oublier la réalité pharmacologique : il s'agit d'une molécule puissante qui agit sur des mécanismes hormonaux fondamentaux. Comme tout médicament actif, il s'accompagne d'un cortège d'effets indésirables potentiels dont les patients doivent être parfaitement informés avant d'entamer le traitement. La transparence sur ces effets est cruciale pour maintenir un équilibre bénéfice/risque favorable.
La communication autour du lancement a mis l'accent sur la commodité et l'efficacité, mais la liste des effets secondaires rapportés lors des essais cliniques est longue et parfois lourde de conséquences. Il est impératif de démystifier ces effets pour éviter que les patients ne soient pas surpris ou effrayés une fois le traitement entamé, ce qui pourrait conduire à un arrêt prématuré et donc à l'échec de la thérapie.
Les troubles digestifs au premier plan
Les effets secondaires les plus fréquemment rapportés avec Foundayo concernent le système digestif. Ce n'est pas une surprise, car la classe des médicaments imitant le GLP-1 agit directement en ralentissant la vidange de l'estomac et en signalant la satiété au cerveau. Cette action mécanique sur le système gastro-intestinal entraîne logiquement des perturbations.
Selon les données issues des essais cliniques, les effets indésirables les plus courants incluent les nausées, la constipation et la diarrhée. Ces symptômes peuvent varier en intensité, allant d'une gêne légère à un inconfort sévère pouvant affecter la qualité de vie quotidienne. D'autres troubles digestifs ont également été observés, tels que des vomissements, des douleurs abdominales, une dyspepsie (mauvaise digestion), une distension abdominale (ballonnements), des éructations, des reflux gastro-œsophagiens et des flatulences.
Ces symptômes apparaissent souvent lors de l'initiation du traitement ou lors de l'augmentation de la dose. C'est pour cette raison que la posologie de Foundayo est progressive : elle débute généralement à 0,8 mg, puis est augmentée par le médecin à 2,5 mg, 5,5 mg et ainsi de suite. Cette montée en charge permet à l'organisme de s'habituer progressivement à la présence de la molécule, réduisant ainsi l'intensité et la fréquence des troubles digestifs. Les médecins jouent ici un rôle crucial de conseil pour aider leurs patients à gérer ces effets secondaires, par exemple en recommandant de manger lentement ou de fractionner les repas.
Risques graves et mise en garde spéciale
Au-delà des désagréments digestifs, Foundayo porte des mises en garde plus sérieuses concernant des risques potentiels plus rares mais graves. La notice du fabricant mentionne explicitement la possibilité de tumeurs de la thyroïde, y compris un cancer de la thyroïde. Cet avertissement est basé sur des observations effectuées lors d'études menées sur des rongeurs, où l'administration de GLP-1 a entraîné l'apparition de tumeurs thyroïdiennes à médullaire (C-cellule).
Bien qu'il n'ait pas été établi de lien de causalité direct chez l'homme, cette potentielle toxicité impose une vigilance extrême. Les patients ayant des antécédents personnels ou familiaux de cancer médullaire de la thyroïde ou de néoplasie endocrinienne multiple de type 2 (NEM 2) ne doivent généralement pas prendre ce type de médicament. Il est donc impératif que le médecin traitant interroge minutieusement le patient sur ses antécédents médicaux familiaux avant de prescrire Foundayo.
D'autres effets secondaires moins fréquents mais notables ont été rapportés, tels que des maux de tête (céphalées), une fatigue importante et, fait plus surprenant, une chute de cheveux (alopécie). Cette perte de cheveux, bien que généralement temporaire, peut être psychologiquement difficile pour les patients déjà en proie à des complexes liés à leur image corporelle. Là encore, l'information et le soutien médical sont essentiels pour accompagner le patient à travers ces changements physiques parfois déstabilisants.
Conclusion : L'ère de l'industrialisation thérapeutique
L'approbation de Foundayo en cinquante jours marque indéniablement un tournant dans l'histoire de la régulation des médicaments. Au-delà de la simple pilule minceur, c'est le modèle de validation des thérapeutiques qui se trouve transformé sous nos yeux. Le programme CNPV, initialement conçu comme un outil d'urgence, semble désormais s'installer comme un mécanisme permanent d'accélération pour les molécules jugées stratégiques. Nous passons d'une logique de patience scientifique à une logique de réactivité industrielle, où la nécessité économique dicte le tempo de la sécurité sanitaire.
Cette évolution préfigure une nouvelle ère que l'on pourrait qualifier d'« Uberisation » de l'accès aux médicaments, inspirant peut-être d'autres domaines comme l'odontologie avec ce traitement japonais testé sur humain. Le succès de Foundayo nous force à nous poser une question essentielle : cette souplesse bureaucratique est-elle la bienvenue pour lutter contre l'épidémie d'obésité, ou ouvrons-nous la boîte de Pandore d'une médecine validée à la va-vite ? Si la rapidité est séduisante, elle ne doit jamais faire oublier que derrière chaque pilule, il y a la santé d'êtres humains. L'avenir nous dira si ce pari audacieux sur la vitesse se soldera par une victoire de la santé publique ou par de regrettables erreurs de casting.