L'idée que perdre une dent est une sentence définitive pourrait bientôt appartenir au passé. Pour des millions de Français, l'édentement n'est pas seulement une inquiétude esthétique, mais un calvaire quotidien qui affecte l'alimentation et la confiance en soi, souvent résolu par des implants coûteux. Pourtant, la nature aurait peut-être prévu une solution de secours que nous ignorons depuis des siècles. Au Japon, des chercheurs sont sur le point de prouver que sous nos gencives sommeille un potentiel insoupçonné, prêt à être réveillé. Ce n'est plus de la science-fiction, mais une réalité clinique qui pourrait redéfinir la médecine dentaire d'ici 2030.
Une troisième rangée de dents existe-t-elle sous vos gencives ?
Contrairement au dogme populaire qui enseigne que l'humain est condamné à ne posséder que deux dentitions au cours de sa vie, la réalité biologique est plus nuancée. Nous sommes programmés, génétiquement, pour posséder les bourgeons d'une troisième génération dentaire, mais ceux-ci restent en sommeil, bloqués par des mécanismes inhibiteurs précis. Cette découverte fascinante renverse notre compréhension du développement humain et suggère que la faculté de régénération n'a pas totalement disparu de notre patrimoine génétique, mais qu'elle a simplement été « mise en veille ». Pour les chercheurs, il ne s'agit pas de créer de nouveaux organes de toutes pièces, mais de libérer un potentiel déjà existant, caché sous la muqueuse gingivale.
Cette révélation ouvre des perspectives vertigineuses pour traiter la fatalité dentaire qui pèse sur une large part de la population. L'absence de repousse naturelle chez l'adulte force aujourd'hui à recourir à des prothèses ou des implants, solutions artificielles qui, bien qu'efficaces, ne restituent pas la sensation biologique de la dent naturelle. Si l'on parvient à activer ces réserves dormantes, nous pourrions assister à une véritable révolution thérapeutique, où le corps serait capable de réparer ses propres dommages dentaires, un concept qui s'inscrit dans la mouvance plus large de la régénération du cartilage ou d'autres tissus.
Pourquoi les reptiles renouvellent-ils leurs dents et pas nous ?
Pour comprendre pourquoi nous n'arrivons pas à renouveler notre sourire, il faut se tourner vers l'évolution et comparer notre destinée à celle des reptiles. Ces derniers bénéficient d'une dentition polyphyodonte, un mécanisme biologique leur permettant de remplacer leurs dents continuellement tout au long de leur existence. Chaque fois qu'une dent est perdue ou usée, un nouveau germe se met en place pour la remplacer, assurant ainsi une fonction masticatoire perpétuelle. L'humain, quant à lui, est né avec une dentition diphyodonte : nous n'avons le droit qu'à deux essais, les dents de lait et les dents définitives.
Cependant, il existe des anomalies biologiques qui prouvent que la frontière n'est pas hermétique. Environ 1 % de la population mondiale souffre d'hyperdontie, une condition caractérisée par l'apparition de dents surnuméraires. Des études, notamment celles menées par l'équipe du Dr Takahashi, ont montré qu'environ un tiers des cas d'hyperdontie ne sont pas de simples accidents génétiques, mais la manifestation spontanée d'une troisième dentition. Ces cas cliniques rares mais réels servent de « preuve de concept » biologique : le matériel génétique nécessaire à la pousse d'une troisième dent est bien présent dans notre ADN, mais il est normalement empêché de s'exprimer.
Quels sont ces bourgeons dormants traqués par le Dr Takahashi ?
À l'origine de cette révolution thérapeutique se trouve le Dr Katsu Takahashi, chef du service de chirurgie buccale à l'Institut de recherche médicale de l'hôpital Kitano à Osaka. Depuis le début de sa carrière, il poursuit une thèse audacieuse : la troisième dentition n'est pas une anomalie, mais une étape développementale qui a été arrêtée prématurément. Ses travaux ont permis de localiser précisément ces bourgeons dentaires dormants, situés sous la gencive adulte, dans un état d'attente qu'il qualifie de « silence biologique ».
Selon le Dr Takahashi, ces structures ne sont pas des reliquats atrophiés sans fonction, mais des organes potentiels parfaitement formés, attendant simplement un signal biochimique spécifique pour se développer. L'enjeu consiste donc à identifier le « code d'accès » qui débloquera ce processus naturel. C'est cette quête du signal activateur qui a conduit son équipe à isoler la protéine USAG-1 comme étant le principal « frein » à cette régénération naturelle. En neutralisant ce frein, le chirurgien espère offrir à l'humanité ce que les reptiles ont conservé : la capacité de se réparer indéfiniment.
USAG-1 : la protéine qui bloque la repousse dentaire
Au cœur de cette innovation médicale se trouve un mécanisme biologique d'une grande complexité, impliquant des protéines agissant comme des interrupteurs génétiques. Le médicament développé par les chercheurs japonais, baptisé TRG035, ne vise pas à créer artificiellement du tissu dentaire, mais à lever une inhibition naturelle. Tout repose sur l'interaction entre l'USAG-1 (Uterine Sensitization Associated Gene-1), une protéine qui bloque la croissance, et les BMP (Bone Morphogenetic Proteins), des protéines essentielles au développement osseux et dentaire. Le rôle de l'USAG-1 est de se lier aux BMP pour empêcher une prolifération excessive de dents, un mécanisme probablement utile pour stabiliser l'occlusion humaine, mais qui devient handicapant en cas de perte de dent.
La compréhension de ce mécanisme ouvre la voie à une approche thérapeutique extrêmement ciblée. Contrairement aux traitements empiriques du passé, l'administration de TRG035 agit comme une clé dans une serrure moléculaire. L'objectif est de perturber l'interaction entre l'USAG-1 et les BMP, laissant ainsi libre cours aux signaux de croissance. Cette stratégie de « déverrouillage » biologique est ce qui rend le projet si prometteur : il ne s'agit pas d'une greffe étrangère, mais de la réactivation d'un programme génétique interne au patient lui-même.
Comment fonctionne l'anticorps TRG035 ?
Le TRG035 est un anticorps monoclonal conçu spécifiquement pour neutraliser l'action de l'USAG-1. En se liant à cette protéine inhibitrice, l'anticorps l'empêche d'interagir avec les BMP, libérant ainsi ces dernières pour exercer leur fonction anabolique. Une fois libérées, les BMP peuvent stimuler les cellules souches résiduelles et les bourgeons dentaires dormants identifiés par le Dr Takahashi, déclenchant le processus de morphogénèse dentaire. C'est un peu comme si l'on retirait le blocage de sécurité sur une machine prête à démarrer.
L'administration du traitement se fait par voie intraveineuse, une méthode qui assure une diffusion systémique du médicament, nécessaire pour atteindre les sites potentiels de développement dans la mâchoire. Les études précliniques ont montré que cette méthode d'administration permet une action efficace sans nécessiter d'injections locales invasives directement dans la gencive. Ce mode de fonctionnement global suggère que le traitement pourrait être efficace même pour des zones difficiles d'accès, offrant une avancée majeure par rapport aux techniques chirurgicales actuelles qui nécessitent des greffes osseuses ou des implants complexes.
Quels résultats ont convaincu les autorités japonaises ?
Le passage de la théorie à la pratique a nécessité une validation rigoureuse sur des modèles animaux, et les résultats ont été spectaculaires. Initialement testés sur des souris, les chercheurs ont observé une régénération complète des dents absentes, sans effets secondaires notables. Cependant, c'est l'expérience sur le furet qui a véritablement scellé le destin du projet et convaincu les autorités réglementaires japonaises d'autoriser les essais humains. Le furet possède une dentition diphyodonte similaire à celle de l'humain, ce qui en fait un modèle biologique beaucoup plus pertinent que le rongeur.
Lors des essais sur furets, l'administration du traitement a induit la pousse d'une septième dent supplémentaire, positionnée naturellement entre les dents existantes. Le résultat le plus impressionnant concernait la morphologie : cette nouvelle dent n'était pas une excroissance malformée, mais possédait la même forme, la même taille et la même structure que les dents voisines. Cette réussite fonctionnelle et esthétique a prouvé que le mécanisme de guidage de la croissance restait intact malgré l'intervention pharmacologique. Aucun effet secondaire grave n'ayant été rapporté au cours de ces phases expérimentales, la voie vers les essais cliniques sur l'homme était dégagée.
Qui est Toregem BioPharma, la start-up japonaise derrière l'innovation ?
Derrière cette percée scientifique se cache une structure entrepreneuriale née du milieu académique, illustrant le transfert de technologie de la recherche fondamentale vers l'application industrielle. Toregem BioPharma, l'entreprise derrière le médicament, est un spin-off de l'Université de Kyoto, l'une des institutions les plus prestigieuses du Japon. Fondée en mai 2020, la société a été créée spécifiquement pour valoriser les découvertes du Dr Takahashi et transformer des années de recherche fondamentale en un traitement tangible pour les patients.
Cette genèse académique garantit une rigueur scientifique élevée, tout en imposant des défis industriels conséquents. La start-up ne s'est pas contentée de vivre de subsides publics ; elle a structuré sa croissance pour attirer des investisseurs privés et nouer des partenariats stratégiques. À la tête de ce navire, le Dr Honoka Kiso, en tant que CEO, pilote une stratégie qui vise non seulement l'innovation thérapeutique, mais aussi la viabilité économique d'un produit qui, s'il tient ses promesses, sera utilisé par des centaines de millions de personnes à travers le monde. Le modèle de Toregem BioPharma montre que la révolution médicale de demain se joue aussi dans les incubateurs de startups.
Comment le projet est-il passé de l'université au financement ?
Le parcours de Toregem BioPharma est un exemple type de réussite dans l'écosystème de l'innovation japonaise. Après sa fondation, la jeune pousse a réussi à lever 380 millions de yens, soit environ 2,3 millions d'euros, en juillet 2023. Cette manne financière a été cruciale pour passer le cap de la recherche préclinique et entrer dans l'arène coûteuse des essais cliniques. Mais le soutien ne s'arrête pas au secteur privé : l'entreprise bénéficie également du financement de l'AMED (Agence japonaise de recherche médicale et développement), un organisme gouvernemental qui soutient les projets à fort impact sanitaire.
Pour industrialiser la production de son anticorps monoclonal, Toregem BioPharma s'est associée à WuXi Biologics, un géant mondial de la fabrication pharmaceutique contractuelle. Ce partenariat est stratégique : il permet à la startup japonaise de s'appuyer sur une infrastructure de production capable de fournir des quantités massives de médicaments, tout en respectant les normes de qualité internationales (GMP). Sans cette alliance, la production à grande échelle de TRG035 aurait pris des années de retard. Cette structure d'entreprise hybride, entre recherche universitaire, financement public et puissance industrielle privée, est ce qui permet aujourd'hui d'envisager une commercialisation à l'horizon 2030.
Quel est le calendrier prévu pour ce traitement ?
Il est crucial de comprendre que l'actuel essai clinique n'est pas le fruit d'un hasard récent, mais l'aboutissement d'un travail de longue haleine. Les travaux du Dr Takahashi ne datent pas d'hier ; ils s'inscrivent dans un programme de recherche fondamentale qui s'étend sur plus d'une décennie. Cette persistance est la clé de la crédibilité actuelle du projet. Contrairement aux « buzz » médiatiques souvent basés sur des données préliminaires fragiles, le traitement TRG035 s'appuie sur une compréhension profonde des mécanismes moléculaires acquise au fil des années.
Ce long matelas scientifique permet de rassurer les régulateurs et le public sur la solidité de l'approche. Ce n'est pas une tentative scientifique hasardeuse, mais un programme structuré, méthodique et validé à chaque étape. Le fait que Toregem BioPharma fixe déjà une date de commercialisation potentielle pour 2030 démontre une confiance dans leurs données et une maîtrise des étapes réglementaires restantes. C'est cette constance dans l'effort et la rigueur qui pourrait bien permettre au Japon d'être le premier pays au monde à offrir une alternative biologique aux implants dentaires.
Quelles sont les étapes des essais cliniques sur l'humain ?
Le passage à l'essai humain représente le Rubicon de toute recherche médicale. Pour le médicament de repousse dentaire, ce protocole est conçu avec une prudence militaire, la sécurité étant le maître-mot absolu à ce stade précoce. L'étude clinique de Phase I a débuté récemment, avec des fenêtres temporelles situées entre juillet et septembre 2024 selon les sources. Ce décalage s'explique par les procédures administratives et logistiques inhérentes aux essais médicaux. L'objectif de cette phase n'est pas encore de prouver l'efficacité esthétique, mais de confirmer que le médicament ne présente pas de toxicité dangereuse pour l'organisme humain.
Le design de cet essai est extrêmement encadré pour maximiser la pertinence des données recueillies tout en minimisant les risques pour les participants. Les données cliniques réelles restent confidentielles pour le moment, protégées par le secret industriel et médical en attendant les premières publications ou communications officielles. Cette confidentialité est habituelle dans les essais précoces, évitant toute spéculation prématurée qui pourrait influencer les résultats ou créer de faux espoirs chez le public. Cependant, la structure même de cet essai nous renseigne sur la stratégie des chercheurs pour les années à venir.
Comment se déroule la Phase I à l'hôpital Kitano ?
Le protocole actuel se déroule principalement à l'hôpital Kitano d'Osaka, le fief du Dr Takahashi. Il implique un groupe restreint de 30 hommes âgés de 30 à 64 ans. Le choix de ne sélectionner que des hommes pour cette première phase vise à éliminer les variables hormonales féminines qui pourraient complexifier l'analyse des effets secondaires. Un critère de sélection crucial est que chaque participant doit manquer d'au moins une dent postérieure. Cette exigence permet de disposer d'un site de mesure clair pour observer une éventuelle repousse, sans attendre des années qu'une dent tombe naturellement.
La durée de l'essai est fixée à onze mois, une période jugée suffisante pour observer la tolérance immédiate et les premiers signes d'activité biologique. Les chercheurs surveilleront de près la réponse de l'organisme à l'administration intraveineuse de TRG035, en analysant le sang et les tissus gingivaux. Si cette première phase confirme l'innocuité du produit, elle ouvrira la porte à des phases plus vastes. La prudence est de mise : même si les résultats sur le furet étaient excellents, le corps humain peut réagir de manière imprévisible, ce qui justifie cette approche progressive par paliers de sécurité.
Qui seront les prochains patients après les adultes ?
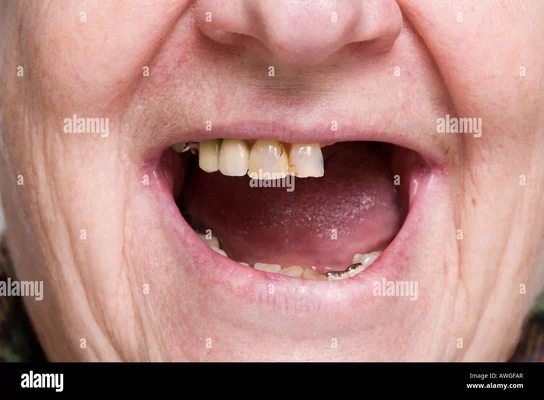
Si la Phase I chez l'adulte est concluante, la stratégie de Toregem BioPharma prévoit une transition rapide vers une population pédiatrique. La prochaine étape ciblera les enfants âgés de 2 à 7 ans souffrant d'anodontie congénitale, une condition rare et dévastatrice où les enfants naissent avec peu ou pas de dents du tout. Pour ces patients, l'enjeu est vital : sans dents, l'apprentissage de la mastication et le développement de la parole sont gravement compromis, ainsi que la structure de la mâchoire. Faire repousser des dents naturelles chez ces enfants serait une victoire médicale et humaine inestimable.
À plus long terme, l'ambition est d'élargir l'indication au grand public. L'objectif final est que le médicament puisse être administré à toute personne ayant perdu une dent, que ce soit à cause d'une carie, d'un traumatisme ou d'une maladie parodontale. Le Dr Takahashi envisage un futur où l'on pourrait simplement se faire une piqûre après une extraction pour voir la dent repousser naturellement. Selon le calendrier actuel, si les essais se déroulent sans accroc, la mise sur le marché commercial est visée pour l'année 2030. Cela nous laisse encore quelques années de patience avant de voir ce traitement arriver dans les cabinets français.
Quelle est la réaction des chirurgiens-dentistes français ?
L'annonce de ces essais japonais a traversé les frontières et suscité des réactions vives au sein de la communauté odontologique française. Si l'espoir est palpable, il est tempéré par une prudence professionnelle de rigueur. Les praticiens français, confrontés quotidiennement aux réalités cliniques de l'édentement, connaissent la complexité de la reconstruction dentaire. Pour eux, une dent n'est pas seulement un organe qui pousse, mais une pièce d'ingénierie biologique complexe qui doit s'articuler parfaitement avec ses voisines et résister à des forces de mastication considérables.
Cet enthousiasme mesuré se justifie par l'expérience. Les chirurgiens-dentistes ont vu défiler de nombreuses « révolutions » promettant la fin de la carie ou la régénération magique de l'émail, qui se sont souvent heurtées au mur de la réalité clinique. Le scepticisme est donc un garde-fou nécessaire. Toutefois, l'ampleur des publications scientifiques et la crédibilité des institutions japonaises impliquées forcent le respect. Les experts français suivent le dossier de près, prêts à saluer la réussite, mais en attendant des preuves irréfutables d'efficacité et d'innocuité à long terme.
Quelles sont les inquiétudes du Dr Lequart (UFSBD) ?
Le Dr Christophe Lequart, chirurgien-dentiste et porte-parole de l'Union Française pour la Santé Bucco-Dentaire (UFSBD), a souligné les nombreuses zones d'ombre qui subsistent. Son inquiétude principale porte sur la qualité et la morphologie des dents régénérées. Si l'expérience sur le furet a montré une dent parfaitement formée, le transfert à l'homme n'est pas garanti. Le Dr Lequart rappelle que lors des premières observations chez l'animal, les formes des nouvelles dents pouvaient parfois être « un peu aléatoires », avec des variations inquiétantes.
Il insiste sur un point crucial : le potentiel existe dans la gencive, mais le déclenchement du processus n'est pas totalement maîtrisé. Une dent qui pousserait de travers, trop petite ou avec une racine trop courte, serait un échec fonctionnel et pourrait créer des problèmes d'occlusion plus graves que l'absence de dent. « On ne sait pas à quoi vont ressembler ces dents qui vont pousser », a-t-il déclaré, soulignant le manque de recul sur la robustesse de ces organes régénérés. Pour un praticien, avoir une dent qui tient dans le temps est aussi important que d'en avoir une tout court.
Pourquoi le pas restant à franchir est-il immense selon les experts ?
Cette prudence est partagée par le monde de la recherche académique française. Le professeur Anne Poliard, de l'Université Paris Cité, qui travaille elle-même sur la repousse dentaire via d'autres voies comme les cellules souches, met en garde contre l'optimisme excessif. Pour elle, la preuve que cela fonctionne chez l'animal existe, mais rien ne garantit que le mécanisme se traduira de manière identique chez l'humain. La biologie humaine a souvent montré qu'elle pouvait réserver des surprises là où les modèles animaux prédisaient un succès.
Marjolaine Gosset, présidente scientifique de l'Institut français pour la recherche odontologique (IFRO), abonde dans ce sens en qualifiant le pas restant à franchir d'immense. Elle insiste sur la nécessité impérative de garantir que la dent régénérée ne soit pas seulement un amas de tissu calcifié, mais une dent « fonctionnelle ». Cela signifie qu'elle doit posséder une vascularisation interne (le nerf et les vaisseaux sanguins), une racine solide ancrée dans l'os, et un émail capable de résister à l'acidité et à l'abrasion. Sans ces paramètres validés, le traitement, même s'il fait repousser de la matière, n'aura que peu d'intérêt clinique réel.
Combien coûtera le traitement comparé aux implants ?
Au-delà des aspects purement médicaux, l'arrivée potentielle d'un médicament de repousse dentaire bouleverse l'économie de la santé bucco-dentaire. En France, la perte d'une dent est synonyme de dépenses importantes, souvent mal remboursées par la sécurité sociale. Aujourd'hui, le « gold standard » pour remplacer une dent manquante reste l'implant dentaire, une vis en titane fixée dans l'os maxillaire. Si cette technique a fait ses preuves et est très fiable, elle reste un investissement financier conséquent pour le patient, ce qui limite son accès à une partie de la population.
L'arrivée d'un traitement biologique comme le TRG035 pourrait donc créer une nouvelle concurrence entre le « tout prothétique » et le « tout biologique ». Si le médicament s'avère moins cher qu'un implant, il pourrait démocratiser la réparation dentaire. Mais si les coûts de développement sont répercutés sur le prix de vente, le traitement pourrait rester onéreux et réservé, au moins dans un premier temps, aux patients aux moyens les plus aisés ou bénéficiant de prises en charge spécifiques. C'est un aspect crucial que les autorités de santé devront surveiller de près pour éviter une fracture dentaire supplémentaire.
Quel est le prix d'un implant dentaire en 2026 ?
Pour comprendre les enjeux économiques, il faut se pencher sur la grille tarifaire actuelle. En 2026, le coût moyen d'un implant dentaire en France se situe dans une fourchette élevée. La Sécurité sociale considère la pose de l'implant et du pilier comme des actes hors nomenclature. En clair, elle ne rembourse pas la vis en elle-même ni son ancrage dans l'os. Seule la couronne prothétique qui vient recouvrir l'implant bénéficie d'un remboursement partiel, fixé à 60 % sur une base de 120 euros, soit environ 72 euros remboursés par la Sécurité sociale.
Pour le patient, cela signifie un reste à charge moyen par dent compris entre 1 500 € et 2 500 €, selon la complexité du cas et la région géographique. Pour une jeune personne active sans une mutuelle haut de gamme couvrant ces soins hors nomenclature, c'est un investissement lourd, souvent différé ou reporté. Face à ces chiffres, l'attente d'un médicament capable de faire repousser la dent pour une fraction de ce prix est compréhensible. C'est ce gouffre financier qui motive tant d'intérêt et d'espoir autour des essais japonais, car une solution biologique pourrait théoriquement alléger considérablement la facture des soins dentaires lourds.
Le traitement sera-t-il plus accessible qu'un bridge ?
À l'heure actuelle, aucun tarif n'a été communiqué par Toregem BioPharma concernant le prix final du traitement TRG035. Il est donc impossible de donner un chiffre précis, mais on peut analyser les indicateurs structurels. La production via WuXi Biologics suggère une capacité de fabrication à échelle industrielle, ce qui permet généralement de réduire les coûts unitaires par rapport à des fabrications artisanales ou en laboratoire. Les traitements par anticorps monoclonaux sont traditionnellement coûteux à développer, mais leurs prix tendent parfois à baisser une fois que les brevets et les infrastructures sont amortis.
Pour évaluer l'accessibilité future, on peut le comparer au coût d'autres traitements biologiques lourds, comme la greffe osseuse ou l'orthodontie complexe. Si le traitement nécessite une seule injection ou une série limitée, il pourrait être compétitif face au prix d'un implant. En revanche, si des doses répétées sont nécessaires sur le long terme, le coût pourrait grimper rapidement. La question du remboursement par la Sécurité sociale française sera également déterminante : le médicament sera-t-il classé comme un soin d'intérêt majeur ou comme un confort esthétique ? C'est la réponse à cette question qui définira si le « troisième sourire » sera pour tous ou pour quelques-uns.
Conclusion : 2030, l'année où perdre une dent ne sera plus une fatalité
L'horizon de 2030 se profile désormais comme une date charnière dans l'histoire de l'odontologie. Ce que nous observons aujourd'hui avec les essais du Dr Takahashi dépasse la simple découverte d'un nouveau médicament : c'est l'aube d'une ère où la médecine régénérative pourrait remplacer la médecine de substitution. La perspective de ne plus avoir recours à de la visserie titanesque pour réparer notre corps, mais de stimuler ses propres capacités de réparation, marque un tournant philosophique et scientifique majeur.
Cependant, il faut garder la tête froide. Le chemin entre les premiers essais sur 30 patients et une disponibilité mondiale dans les pharmacies est encore long et semé d'embûches. Les réserves formulées par les experts français concernant la forme, la robustesse et l'insertion des nouvelles dents sont des garde-fous essentiels. Si l'année 2030 devrait théoriquement voir la commercialisation de ce traitement au Japon, son arrivée en France pourrait prendre du temps supplémentaire, en attendant les validations des autorités sanitaires européennes.
Néanmoins, l'espoir est désormais tangible. Pour les millions de personnes qui redoutent le fauteuil du dentiste et les factures exorbitantes, cette innovation promet un avenir où la perte d'une dent ne sera plus un traumatisme irréversible, mais un incident banal et temporaire. Tant que l'on n'aura pas les résultats définitifs des essais en cours, la prudence reste de mise, mais l'humanité n'a jamais été aussi proche d'effacer la condamnation biologique de l'édentement. Dans quelques années, peut-être, sourire à pleine dent sera un droit que l'on pourra reconquérir à tout âge.


