Imaginez un instant qu'une malédiction biologique, semblable à celles que l'on croise dans les contes anciens, soit soudainement confirmée par la science moderne. Pas une formule magique, mais une molécule chimique synthétique qui, administrée une seule fois à une mère, condamne sa descendance à souffrir de maladies pendant des siècles. C'est pourtant la réalité vertigineuse mise en lumière par les travaux du laboratoire de Michael Skinner à la Washington State University. Une étude publiée en 2026 démontre qu'une exposition brève à un fongicide courant, le vinclozoline, suffit à programmer des pathologies qui se transmettent intactes sur vingt générations de rats, sans aucune nouvelle exposition. Ce constat défie notre intuition classique de l'hérédité et nous force à reconsidérer notre rapport à l'environnement chimique : nous ne sommes pas les seuls maîtres de notre destin biologique, car nous portons en nous l'écho lointain des décisions passées.
Une expérience qui défie l'intuition génétique
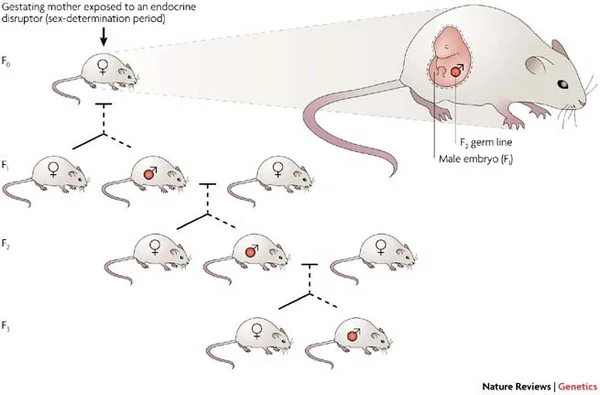
Pour parvenir à cette conclusion stupéfiante, l'équipe de chercheurs a conçu un protocole d'une rigueur implacable. Des rates gestantes (la génération F0) ont été exposées au vinclozoline pendant une fenêtre temporelle extrêmement précise et courte : seulement sept jours, entre le huitième et le quatorzième jour de leur gestation (E8-E14). Ce moment n'a pas été choisi au hasard ; il correspond à la période critique de la détermination sexuelle des gonades chez le fœtus, là où s'élaborent les cellules germinales futures, les « graines » de la prochaine génération. À partir de là, plus aucune goutte de pesticide n'a été administrée à aucun animal, ni aux parents, ni aux enfants, ni aux petits-enfants. Pourtant, les chercheurs ont suivi la lignée jusqu'à la vingtième génération, observant la persistance de maladies graves avec une régularité métronomique.
Ce qui rend cette observation si fascinante, c'est la stabilité de cette transmission biologique. Comme l'explique Michael Skinner, biologiste à la WSU et directeur fondateur du Center for Reproductive Biology, « une fois que cette information est programmée dans la lignée germinale, elle devient aussi stable qu'une mutation génétique ». Cela signifie que l'information pathologique ne se dilue pas, ne s'atténue pas au fil des croisements, mais se transmet avec la même fidélité qu'une séquence d'ADN codée pour la couleur des yeux. L'étude, publiée dans la revue PNAS, démontre que l'empreinte laissée par le poison résiste obstinément à l'usure du temps biologique, contredisant l'idée reçue que la lignée germinale est un sanctuaire inviolable qui efface les cicatrices du passé à chaque nouvelle génération.
Quand le corps humain n'appartient plus qu'à lui-même
Cette découverte nous confronte à une réalité philosophique vertigineuse : le concept de « souveraineté du corps » est peut-être une illusion. Nous avons tendance à penser que notre santé est le résultat de notre mode de vie actuel — ce que nous mangeons, notre activité physique, nos choix immédiats. Or, cette étude suggère que notre biologie peut être programmée par des événements survenus bien avant notre naissance, voire avant la naissance de nos arrière-grands-parents. Si nous transposons ce concept à l'humain, cela signifie que certaines de nos fragilités actuelles ne sont peut-être pas les nôtres, mais un héritage toxique légué par des expositions environnementales anciennes.
Nous sommes, malgré nous, les porteurs silencieux d'une histoire que nous n'avons pas vécue, remettant en cause l'idée même d'individualité biologique. Si l'environnement d'un ancêtre peut modifier l'expression des gènes de ses descendants lointains, alors la frontière entre l'individu et son milieu devient poreuse. Nous ne sommes pas des entités closes, évoluant indépendamment de notre environnement historique, mais des nœuds dans un réseau biologique complexe où les actions passées continuent de résonner dans le présent. Cette prise de conscience oblige à reconsidérer la responsabilité individuelle : sommes-nous vraiment responsables de toutes nos faiblesses, ou sommes-nous les victimes involontaires des choix chimiques de nos prédécesseurs ?
Vinclozoline : le perturbateur endocrinien qui a traversé nos campagnes
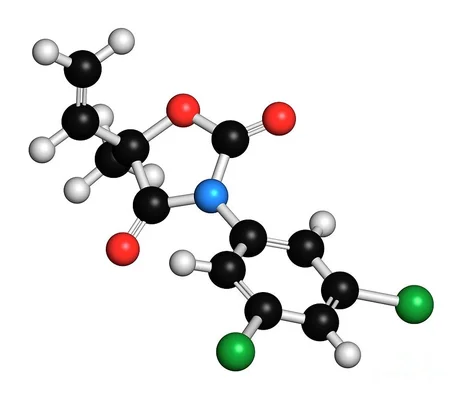
Le « méchant » de cette histoire est une molécule chimique nommée vinclozoline. Longtemps utilisé dans l'agriculture intensive, ce fongicide a été conçu pour protéger les cultures, notamment les vignes, contre les ravages des moisissures. Pourtant, sa structure chimique lui confère une propriété insidieuse : il agit comme un perturbateur endocrinien puissant, capable de brouiller les messages hormonaux essentiels au développement des organismes vivants. Bien que l'étude se concentre sur des rats de laboratoire, le vinclozoline a été largement déployé dans nos campagnes, exposant indirectement les populations humaines via la chaîne alimentaire, soulevant des questions inquiétantes sur notre passé agricole et ses résidus invisibles.
Un fongicide conçu pour les vignes, pas pour les corps humains
Le vinclozoline appartient à une classe de produits chimiques développés pour tuer ou inhiber la croissance de champignons parasites, particulièrement ceux qui s'attaquent aux raisins de cuve dans l'industrie du vin. Son efficacité agronomique a conduit à son adoption massive avant que l'on ne mesure pleinement ses effets collatéraux sur le système endocrinien. Le problème majeur réside dans son mécanisme d'action : il s'agit d'un anti-androgène. En termes simples, cette molécule est capable de se lier aux récepteurs des androgènes — les récepteurs de la testostérone et d'autres hormones masculines — et de bloquer leur action.
Comme le détaillent des analyses toxicologiques publiées par le Centre International de Recherche sur le Cancer, le vinclozoline est même métabolisé par l'organisme en composés encore plus actifs, qui se fixent sur ces récepteurs avec une affinité redoutable, empêchant les hormones naturelles de jouer leur rôle crucial dans le développement sexuel et la reproduction. L'exposition prénatale à ce composé est donc particulièrement critique car elle intervient au moment où le fœtus se construit, brouillant les signaux hormonaux nécessaires à une différenciation sexuelle correcte et à la mise en place des organes reproducteurs. C'est cette interférence moléculaire précise qui déclenche la cascade d'événements menant aux maladies observées chez l'adulte.
Pourquoi les perturbateurs endocriniens sont des « faux messagers »
Pour saisir la dangerosité du vinclozoline, il faut comprendre ce qu'est un perturbateur endocrinien. Imaginez votre système hormonal comme un réseau de communication complexe reliant le cerveau aux organes, utilisant des hormones comme des messages précis pour réguler la croissance, le métabolisme ou la reproduction. Un perturbateur endocrinien est comme un espion qui intercepterait ce réseau : il ressemble suffisamment au message original pour tromper le récepteur, mais au lieu de transmettre l'information correcte, il le brouille ou le bloque.
Le vinclozoline envoie un signal de « silence » aux récepteurs de testostérone, paralysant des processus vitaux. Cette interférence est particulièrement alarmante quand on sait à quel point les hormones sexuelles sont sensibles, même à doses infimes. Ce « faux message » chimique explique pourquoi l'exposition à ces molécules est soupçonnée d'être liée à la baisse globale de la fertilité masculine et à l'augmentation de certains cancers hormono-dépendants observés depuis quelques décennies. Contrairement à un poison classique qui tuerait la cellule, le perturbateur endocrinien la « reprogramme » subtilement, laissant l'organisme en vie mais fonctionnant mal, un dysfonctionnement qui peut se propager silencieusement à travers les générations via la lignée germinale.
Épigénétique : quand l'ADN se fait « hacker » sans changer de code
Si le vinclozoline provoque des maladies sur vingt générations sans altérer la séquence de l'ADN, comment est-ce possible ? La réponse réside dans un domaine fascinant de la biologie moderne : l'épigénétique. Contrairement à la génétique classique, qui étudie la séquence des lettres qui composent notre code génétique (l'ADN), l'épigénétique s'intéresse à la manière dont ce code est lu, utilisé ou verrouillé par la cellule. On peut utiliser l'analogie d'un ordinateur : le matériel (l'ADN) reste le même, mais c'est le logiciel ou les paramètres de configuration (l'épigénome) qui déterminent quelles applications fonctionnent et lesquelles sont désactivées. L'étude de Skinner montre qu'une exposition toxique peut corrompre ces paramètres, et que cette corruption se copie et se colle d'une génération à l'autre.
Méthylation : les « marqueurs » qui désactivent nos gènes
Au cœur de ce mécanisme se trouve un processus appelé méthylation de l'ADN. Imaginez que chaque gène de votre ADN possède un petit interrupteur. Lorsqu'un groupe chimique appelé « groupe méthyle » se fixe sur l'ADN à un endroit précis, c'est comme si l'on éteignait l'interrupteur : le gène est toujours là physiquement, mais il ne peut plus s'exprimer, il est « éteint » ou silencieux. L'exposition au vinclozoline pendant le développement fœtal provoque l'apparition de ces marques épigénétiques anormales, que les chercheurs appellent des « régions méthylées de manière différentielle » (DMR).
Ces modifications touchent spécifiquement des gènes impliqués dans la régulation du métabolisme, de la reproduction ou de la croissance cellulaire. Ce qui est terrifiant, c'est que ces marques, une fois posées sur les cellules germinales, ne s'effacent pas lors de la fécondation. Elles sont transmises telles quelles à l'embryon suivant, perpétuant ainsi la « programmation » de la maladie bien que le code ADN lui-même reste intact. Ce processus de méthylation anormale agit comme une ombre portée sur le génome, dictant quelles parties de notre patrimoine génétique doivent être utilisées et lesquelles doivent rester cachées, orientant ainsi le développement de l'organisme vers la pathologie plutôt que vers la santé.
Pourquoi la lignée germinale mâle est le véhicule du « fantôme »
Une découverte cruciale de ces travaux est la prédominance de la transmission par la lignée germinale mâle. Ce sont les spermatozoïdes qui véhiculent cette information épigénétique altérée vers la génération suivante. Lorsqu'un fœtus mâle est exposé au vinclozoline (entre E8 et E14), ses propres cellules germinales — celles qui donneront un jour ses spermatozoïdes — sont en plein développement. Le poison agit donc sur deux niveaux : l'individu exposé (F1), et ses futurs enfants (F2) via ses spermatozoïdes déjà programmés.
Les études du laboratoire Skinner ont montré que ce sont les ARN non codants, de petites molécules d'ARN qui ne codent pas pour des protéines mais régulent l'expression des gènes, qui sont également perturbés dans les spermatozoïdes. Plus spécifiquement, les chercheurs ont identifié des modifications dans les petits ARN non codants, notamment les fragments d'ARN de transfert (tRFs), qui sont des régulateurs clés de l'expression génétique au début du développement embryonnaire. Ainsi, le mâle transmet une « notice de montage » défectueuse à sa descendance, une notice qui dictera comment l'ADN doit être lu, entraînant l'apparition de maladies à l'âge adulte, comme des troubles de la prostate ou des anomalies rénales, plusieurs générations plus tard. La lignée mâle devient donc le vecteur silencieux d'une mémoire toxique que la lignée femelle ne transmet pas avec la même efficacité dans ce modèle.
Vingt générations de rats : une dette biologique de cinq siècles
Pour saisir l'ampleur véritable de cette découverte, il est indispensable de traduire l'échelle temporelle du rongeur à celle de l'homme. Dire « vingt générations » reste abstrait tant que l'on ne l'a pas mis en perspective avec notre propre histoire. Cette durée représente une échelle de temps vertigineuse qui dépasse largement la vie d'un individu, voire d'une société ; c'est une véritable dette biologique qui se paye sur des siècles. Si l'on transpose ces résultats au rythme de reproduction humaine, cela signifie qu'une décision prise par un arrière lointain, il y a plusieurs centaines d'années, pourrait encore dicter l'état de santé de vos enfants aujourd'hui. C'est un saut temporel qui lie le passé le plus lointain à notre présent biologique de manière indissoluble.
Le calcul qui fait froid dans le dos
Faisons le calcul ensemble pour mesurer l'impact de cette « malédiction » temporelle. Chez le rat de laboratoire, une génération — le temps séparant la naissance d'un parent de la naissance de sa progéniture — est très courte, approximativement de trois à quatre mois. L'étude menée sur vingt générations s'étend donc sur une période de cinq à sept ans d'observation continue chez l'animal. Maintenant, changeons d'échelle et appliquons cela à l'espèce humaine, où une génération est généralement estimée à vingt-cinq ans. Vingt générations d'humains représentent environ 500 ans.
Pour nous donner un repère historique concret, il faut remonter à l'année 1510, sous le règne de François Ier, pour trouver l'ancêtre commun dont les expositions nous affecteraient encore en 2026. Si un roi de la Renaissance avait été exposé à un produit similaire, nous en subirions aujourd'hui les conséquences sanitaires, ignorant tout de la cause originelle. Cette perspective transforme notre vision de l'histoire médicale : nous ne sommes pas seulement les héritiers des gènes de nos ancêtres, mais aussi des expositions environnementales qu'ils ont subies. La « flèche du temps » biologique est bien plus longue que la flèche de notre mémoire consciente, et nous portons des charges que l'histoire a oubliées mais que notre corps se rappelle.
Les maladies qui traversent les siècles sans perdre en virulence
Le plus effrayant dans cette transmission transgénérationnelle n'est pas seulement sa durée, mais la stabilité des pathologies observées. L'étude rapporte que les rats de la F3, F4, et jusqu'à la F20 génération développent des maladies avec une incidence similaire à la première génération exposée. Il ne s'agit pas de maux mineurs ou bénins. Le tableau clinique est lourd : on observe une prévalence élevée de troubles de la prostate, d'anomalies rénales sévères, de dysfonctionnements du système immunitaire rendant les animaux plus vulnérables, ainsi que le développement de tumeurs.
De plus, les mâles montrent une augmentation de l'apoptose (la mort programmée) des cellules spermatogéniques, ce qui réduit leur fertilité. Ces maladies ne s'atténuent pas avec le temps, comme le ferait une dilution génétique classique ; elles persistent, « gravées dans le marbre » épigénétique, prouvant que la dette biologique ne s'efface pas avec le temps qui passe. L'étude de PNAS confirme que la stabilité de ces modifications épigénétiques est comparable à celle des mutations génétiques. Cela implique que sans intervention extérieure ou sans sélection naturelle forte éliminant les individus porteurs de ces marques, la « malédiction » peut se perpétuer indéfiniment, transformant une erreur temporaire de l'histoire en une fatalité biologique permanente pour la lignée.
Interdit en Europe depuis 2007 : pourquoi le danger persiste
Face à un tel constat scientifique, la réaction logique serait de penser que le danger a été écarté par une interdiction stricte. En effet, l'Union Européenne a réagi avec fermeté en interdisant le vinclozoline. Cependant, la réalité est plus complexe et plus sombre. L'interdiction dans une partie du monde n'efface pas la présence ubiquitaire de la molécule, ni son usage continu ailleurs. De plus, la nature même de l'épigénétique suggère que les dégâts causés par des décennies d'utilisation peuvent être déjà inscrits dans la lignée germinale de populations entières, rendant l'interdiction nécessaire mais insuffisante pour effacer le tableau clinique futur.
L'Europe a tiré un trait, mais pas la planète
Soyons justes : l'Europe a pris la mesure du danger relativement tôt. Selon les textes officiels du Journal Officiel de l'Union Européenne, les États membres étaient obligés de retirer les autorisations des produits phytopharmaceutiques contenant du vinclozoline à compter du 1er janvier 2007. D'autres nations, comme l'Australie et l'Afrique du Sud, ont emboîté le pas. Pourtant, comme le soulignent les rapports de l'IARC, l'utilisation de ce produit a simplement été restreinte aux États-Unis et continue de diminuer sans pour autant disparaître.
Plus inquiétant encore, il est toujours utilisé dans d'autres pays du monde, souvent là où les réglementations environnementales sont plus laxistes. Nous vivons dans un écosystème globalisé : interdire un poison chez soi ne nous protège pas totalement si l'on continue d'importer des aliments traités avec ce même poison depuis l'étranger. La circulation mondiale des marchandises crée une faille dans la défense sanitaire : une molécule bannie dans nos champs peut revenir dans notre assiette via l'importation de fruits, de légumes ou de vins produits dans des régions où elle est encore légale. Cette disparité réglementaire mondiale rend la protection des populations extrêmement difficile face à des polluants persistants qui ignorent les frontières.
Les fantômes chimiques dans notre assiette
Même si l'arrêt total de l'utilisation du vinclozoline était décrété demain à l'échelle planétaire, nous devrons composer avec ses « fantômes » chimiques. Ces molécules sont connues pour leur persistance dans l'environnement. Elles peuvent s'incruster dans les sols contaminés des anciens vignobles ou des vergers, contaminant les cultures suivantes même des années après la dernière pulvérisation. De plus, la chaîne alimentaire mondiale est un maillage complexe : des denrées importées, provenant de régions où le vinclozoline est encore autorisé, peuvent se retrouver dans nos assiettes sans que nous en ayons conscience.
Il ne s'agit pas de céder à la panique ou de diaboliser systématiquement notre alimentation, mais de maintenir une vigilance critique. Les résidus de pesticides, même à faibles doses, agissent comme des perturbateurs endocriniens dont l'effet cumulatif sur la lignée germinale reste largement sous-estimé par les modèles toxicologiques actuels. Ces modèles se basent souvent sur des effets aigus ou sur des expositions directes, négligeant l'effet « bombe à retardement » de l'épigénétique transgénérationnelle. Nous sommes exposés à un cocktail chimique dont les effets individuels sont mal connus, et dont les effets combinés sur nos descendants le sont encore moins. C'est une loterie biologique dont nous jouons les numéros sans connaître les règles.
Sommes-nous les héritiers d'une dette biologique invisible ?
Alors que nous refermons ce dossier scientifique vertigineux, une question centrale demeure en suspens, comme un écho persistant : que signifie être humain dans un monde où notre biologie est malléable par des produits chimiques ? L'étude sur le vinclozoline nous force à admettre que nous sommes peut-être, sans le savoir, les dépositaires d'une dette biologique contractée par nos aïeux. Cette « mémoire du corps » transcende notre conscience individuelle et nos choix actuels. Elle nous lie au passé d'une manière bien plus tangible que ne le pourraient jamais les livres d'histoire ou les traditions familiales. Chaque cellule de notre corps pourrait porter la cicatrice invisible d'une exposition subie par un ancêtre lointain.
La mémoire du corps : un héritage qu'on ne peut pas refuser
Cette découverte nous invite à regarder notre santé, et celle de nos proches, sous un jour nouveau. Lorsqu'on observe des tendances inquiétantes, comme la baisse de la fertilité masculine ou l'augmentation de certaines maladies chroniques et auto-immunes comme analysé récemment dans notre dossier sur la mortalité en 2026, il est désormais légitime de se demander quelle part de ces maux relève de l'hérédité génétique classique et quelle part provient de modifications épigénétiques induites par l'environnement. Si nos corps mémorisent ces agressions chimiques, cela signifie que la santé publique ne se joue pas uniquement dans la médecine curative d'aujourd'hui, mais aussi dans la prévention environnementale de demain.
Nous portons un héritage que nous n'avons pas choisi, mais dont nous subissons les conséquences. Cette idée bouleverse la notion même de responsabilité individuelle en santé. Si nous tombons malade à cause d'une exposition épigénétique de notre arrière-grand-mère, sommes-nous responsables ? La société est-elle responsable ? Cette « mémoire du corps » ajoute une couche de complexité éthique au débat sur la santé environnementale. Elle suggère que la pollution d'hier est la maladie d'aujourd'hui, et que l'inaction climatique ou écologique actuelle est une prescription pour la souffrance des générations futures. Nous sommes les gardiens d'un patrimoine génétique et épigénétique qui ne nous appartient pas en propre, mais qui nous est confié pour un temps limité.
Réparer l'héritage : de la conscience à l'action
Pourtant, cette prise de conscience ne doit pas être une source de résignation. Si l'épigénétique nous apprend que des facteurs environnementaux peuvent programmer la maladie négativement, elle suggère aussi une voie inversible potentiellement. L'espoir réside dans notre capacité à comprendre ces mécanismes pour, peut-être un jour, les « déprogrammer » ou les réparer. L'interdiction du vinclozoline en Europe est une victoire de la précaution qui aura des effets bénéfiques sur les siècles à venir. Elle nous rappelle que chaque décision politique aujourd'hui est un acte biologique pour l'avenir.
Face aux perturbateurs endocriniens actuels qui pullulent dans notre environnement — plastiques, cosmétiques, pesticides modernes — nous devons faire preuve d'une vigilance absolue. La science nous a donné la preuve que nos actes ont des répercussions éternelles sur le vivant ; à nous de nous montrer dignes de cette responsabilité historique. La recherche se tourne maintenant vers des solutions pour nettoyer l'épigénome, pour effacer ces marques indésirables et briser le cycle de la maladie transgénérationnelle. D'ici là, la meilleure arme dont nous disposons reste la prévention et le principe de précaution. Protéger l'environnement, c'est littéralement protéger l'ADN de nos enfants et de leurs enfants, en s'assurant que nous ne leur léguons pas une notice de montage sabotée.
Conclusion
L'étude menée sur le vinclozoline par l'équipe de Michael Skinner à la Washington State University marque un tournant décisif dans notre compréhension de la biologie. En démontrant qu'une exposition ponctuelle à un perturbateur endocrinien peut induire des maladies transmises sur vingt générations, elle brise le dogme selon lequel seules les mutations génétiques peuvent façonner l'hérédité à long terme. Nous ne sommes plus de simples individus isolés, mais des maillons d'une chaîne biologique sensible, capable d'enregistrer et de répercuter les traumatismes environnementaux bien après que la cause première ait disparu. Cette découverte impose une redéfinition radicale de notre responsabilité : protéger l'environnement des polluants chimiques n'est plus seulement une question d'écologie, c'est une urgence médicale pour les générations futures, proches et lointaines. Car, comme nous l'avons vu, une seule erreur peut avoir des conséquences qui résonnent pendant des siècles.