Imaginez un instant pouvoir ranger sa seringue à insuline pour de bon après vingt-cinq ans de dépendance quotidienne. Ce scénario, qui relève encore du rêve pour des millions de personnes, est devenu une réalité clinique poignante en Chine. Une équipe médicale de Shanghai a annoncé une première mondiale : la rémission fonctionnelle d'un diabète de type 2 grâce à une thérapie cellulaire révolutionnaire. Cette avancée ne se contente pas de traiter les symptômes ; elle vise à réparer l'organe défaillant. Toutefois, derrière ce miracle médical se cache une réalité scientifique complexe, des coûts exorbitants et de nombreuses questions éthiques. Plongeons au cœur de cette actualité fascinante qui pourrait redéfinir l'avenir de la médecine régénérative.
Shanghai 2021 : le jour où un patient a définitivement posé sa seringue
L'histoire débute à l'hôpital Changzheng de Shanghai, un lieu qui est désormais entré dans l'histoire de la médecine. En juillet 2021, une procédure chirurgicale d'un genre nouveau y a été menée sur un patient dont le cas médical semblait désespéré. Ce n'est pas une simple greffe d'organe, mais une véritable reconstruction biologique in vivo. Le personnel soignant a suivi ce cas avec une attention particulière, sachant que chaque semaine qui passait sans insuline serait une victoire contre une maladie chronique considérée comme incurable.
L'impact médiatique de cette annonce, publiée dans la revue Cell Discovery au printemps 2024, a été considérable. Pourtant, au-delà des gros titres, c'est l'histoire humaine d'un homme de 59 ans qui nous interpelle. Après un quart de siècle à vivre avec l'épée de Damoclès d'une glycémie instable, ce patient a vu sa vie bouleversée en quelques mois. Ce cas clinique sert de preuve de concept, démontrant qu'il est possible de restaurer la fonction naturelle du pancréas, même après des décennies de défaillance métabolique.
Un cas clinique qui défie 25 ans de maladie
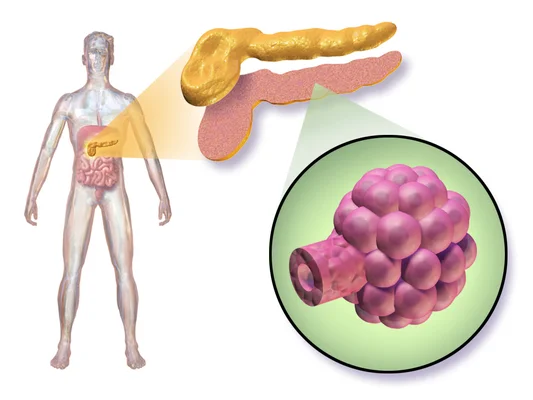
Le protagoniste de cette avancée médicale est un homme de 59 ans dont l'état de santé était critique. Atteint de diabète de type 2 depuis vingt-cinq ans, son corps subissait les ravages cumulés de cette pathologie silencieuse. Sa situation s'était considérablement aggravée suite à une greffe de rein en 2017, rendue nécessaire par l'insuffisance rénale, une complication classique du diabète mal contrôlé. À ce stade, la fonction de ses îlots pancréatiques, ces petites structures responsables de la production d'insuline, était sévèrement compromise, voire inexistante.
Ce profil médical spécifique en a fait le candidat idéal pour une thérapie aussi expérimentale. Étant déjà sous immunosuppresseurs pour protéger son rein transplanté, il présentait un terrain biologiquement « préparé » pour accepter de nouvelles cellules sans les rejeter immédiatement. Les médecins de Shanghai ont vu en lui une opportunité unique de tenter une approche radicale : remplacer le tissu pancréatique défaillant par des cellules souches reprogrammées. C'était un pari audacieux, compte tenu de l'ancienneté de sa maladie et de la fragilité de son organisme.
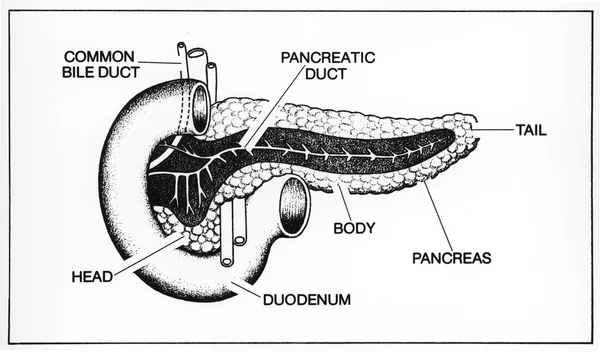
Sevré d'insuline : les 11 semaines qui ont changé tout
La chronologie de cette guérison ressemble à un scénario de science-fiction, pourtant chaque étape a été documentée avec une rigueur scientifique absolue. La transplantation des cellules a eu lieu en juillet 2021, introduisant dans le corps du patient ce que les chercheurs appellent des « îlots pancréatiques endodermiques » (E-islets). La surveillance post-opératoire a été intense, mais les résultats ont dépassé toutes les attentes. Dès la onzième semaine suivant l'intervention, soit moins de trois mois après la chirurgie, le patient a pu se sevrer complètement de ses injections d'insuline.
Ce sevrage rapide n'était qu'une première étape. Les médecins ont continué à le suivre scrupuleusement, observant que son organisme maintenait une glycémie dans la norme sans apport externe d'insuline. Un an plus tard, ce n'était plus seulement l'insuline qui était arrêtée, mais aussi l'ensemble des médicaments oraux antidiabétiques. Trente-trois mois après l'intervention, le patient vit toujours sans traitement spécifique pour le diabète, prouvant que la rémission n'est pas un feu éphémère mais une réalité durable. C'est ce délai de suivi long qui confère à cette étude sa crédibilité incontestable.
Du sang aux îlots pancréatiques : la « recette » scientifique de l'hôpital Changzheng
Comment passe-t-on d'une simple prise de sang à la création d'un organe fonctionnel ? C'est toute la magie de la biologie cellulaire moderne. L'équipe de l'hôpital Changzheng a développé un protocole en plusieurs étapes qui transforme les cellules du patient lui-même en usine à insuline. Ce processus, d'une complexité vertigineuse, repose sur la compréhension fine du développement embryonnaire. L'objectif n'est pas de greffer une cellule magique, mais de mimer la nature en accéléré, guidant des cellules adultes indifférenciées vers leur destinée finale de cellules productrices d'insuline.
Cette approche marque une rupture fondamentale avec les traitements classiques. Au lieu de compenser le manque d'insuline par des injections, on s'attaque à la cause racine du problème : la disparition des cellules bêta du pancréas. C'est la différence entre réparer une roue crevée à chaque kilomètre et changer la roue défectueuse. Grâce aux progrès de la recherche sur les cellules souches, il est désormais possible de recréer ce tissu fonctionnel en laboratoire, ouvrant la voie à une médecine véritablement régénérative et curative.
Reprogrammer ses propres cellules pour éviter le rejet
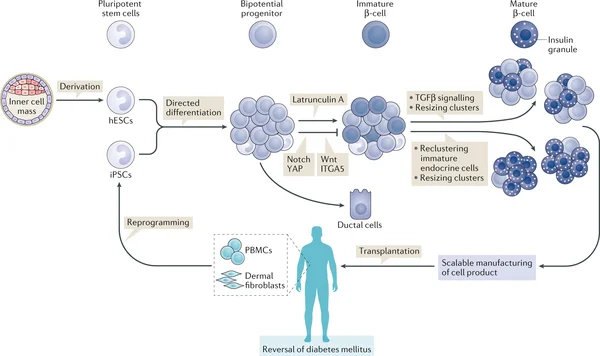
L'innovation majeure de cette thérapie réside dans l'origine des cellules utilisées. Contrairement aux greffes classiques qui nécessitent un donneur compatible, les médecins shanghaïens ont utilisé les propres cellules du patient. Ils ont prélevé des cellules mononucléées de son sang périphérique. Ces cellules ont ensuite subi un processus de reprogrammation pour devenir des cellules souches pluripotentes induites (iPSC). Cela signifie qu'on a « rembobiné » l'horloge biologique de ces cellules pour les ramener à un état proche de l'embryon, capable de se transformer en n'importe quel type de cellule.
Une fois ces cellules souches obtenues, elles ont été guidées pour devenir des cellules souches endodermiques. L'avantage de cette méthode autologue est considérable : puisque les cellules proviennent du patient lui-même, le risque de rejet immunologique est quasi nul. On évite ainsi la nécessité de chercher un donneur rare et de lourds traitements anti-rejet, bien que dans ce cas précis, le patient prenne déjà des immunosuppresseurs pour son rein. Cette technique crée un véritable « bio-médicament » sur mesure, parfaitement adapté à la biologie de l'individu.
Créer un pancréas « artificiel » en laboratoire
L'étape suivante, peut-être la plus spectaculaire, est la différenciation. Les cellules souches sont cultivées dans un environnement artificiel qui reproduit les signaux chimiques du développement pancréatique. Sous l'action de facteurs de croissance spécifiques, elles se transforment en cellules progénitrices pancréatiques, puis finalement en un tissu insulaire fonctionnel, baptisé « E-islets ». Ces cellules s'auto-organisent en structures tridimensionnelles capables de sécréter de l'insuline en réponse au glucose, exactement comme le feraient des îlots naturels.
Cet exploit technique représente une prouesse d'ingénierie biologique. Il ne suffit pas d'avoir les bonnes cellules, il faut qu'elles communiquent entre elles et réagissent correctement aux variations du taux de sucre dans le sang. Le fait que l'équipe chinoise soit parvenue à créer un tissu aussi sophistiqué in vitro prouve que la maîtrise de la différenciation cellulaire atteint un niveau de maturité jamais vu auparavant. Ces îlots synthétiques sont ensuite transplantés dans le corps du patient, où ils s'intègrent et reprennent le travail que le pancréas naturel ne pouvait plus assurer.
116 semaines de surveillance : les chiffres qui prouvent l'efficacité
Pour convaincre la communauté scientifique, il ne suffit pas de raconter une histoire de succès ; il faut apporter la preuve formelle que le patient est guéri. C'est là que l'importance du suivi à long terme entre en jeu. L'étude publiée ne se contente pas d'une anecdote positive sur quelques semaines ; elle s'étend sur 116 semaines, soit plus de deux ans de surveillance médicale rigoureuse. Durant cette période, une batterie de tests biologiques a été réalisée pour vérifier que les nouvelles cellules fonctionnaient correctement et en toute sécurité.
Les données recueillies sont d'une précision chirurgicale et constituent le cœur dur de la publication scientifique. Elles montrent une normalisation progressive et stable des paramètres biologiques, sans les fluctuations chaotiques habituellement observées chez les diabétiques insulino-dépendants. C'est cette stabilité dans le temps qui permet aux chercheurs d'affirmer qu'il s'agit d'une véritable rémission et non d'un phénomène passager. La « Hard Science » parle ici le langage des chiffres, et ces chiffres sont sans appel.
HbA1c et peptide C : la métamorphose biologique
L'indicateur clé de suivi chez les diabétiques est l'hémoglobine glyquée (HbA1c), qui reflète la moyenne de la glycémie sur les trois derniers mois. Avant l'intervention, le patient affichait un taux de 6,6 %, un niveau déjà « contrôlé » grâce à de fortes doses d'insuline, mais témoignant d'une instabilité résiduelle. Après la greffe et le sevrage, ce taux a chuté pour atteindre 4,6 % à la 113e semaine. Un tel chiffre n'est pas seulement bon, il est physiologiquement parfait, indiquant un métabolisme du glucose comparable à celui d'une personne non diabétique.
Mais l'argument le plus probant réside dans le dosage du peptide C. Cette molécule est produite en même temps que l'insuline par le pancréas et son taux dans le sang est le miroir exact de la production d'insuline endogène. Chez ce patient, le taux de peptide C a été multiplié par trois par rapport à son niveau avant l'opération. Cela signifie que les nouvelles cellules greffées ne sont pas en sommeil ; elles sont actives, vivantes et produisent de l'insuline en quantité suffisante pour réguler le sang. C'est la preuve irréfutable que le pancréas a été rétabli fonctionnellement.
Pas de tumeurs, mais quelques effets secondaires gérables
La sécurité est l'autre pilier de cette étude. L'utilisation de cellules souches s'accompagne toujours d'une crainte théorique majeure : le risque de tératome, une tumeur qui peut se former si des cellules souches non différenciées restent dans le greffon. Pour rassurer le monde médical, l'équipe chinoise a réalisé des IRM régulières et dosé des marqueurs tumoraux spécifiques pendant tout le suivi. Le résultat est sans appel : aucune formation tumorale n'a été détectée chez le patient, prouvant que le protocole de purification des cellules est efficace.
Cependant, la procédure n'est pas dénuée d'effets secondaires. Le patient a souffert d'une inflammation localisée au site d'implantation, ainsi que d'une distension abdominale et d'une perte d'appétit temporaire dans les semaines suivant la greffe. Ces symptômes, bien que désagréables, ont été gérés médicalement et se sont résorbés d'eux-mêmes. Le patient a également perdu environ 4 kilos, une perte de poids restituée par la suite. Ces désagréments restent mineurs au regard du bénéfice obtenu : la liberté d'une vie sans insuline et sans la menace constante des complications diabétiques graves.

Un cas isolé ou le début de la fin ? Les mises en garde du corps médical
Face à une telle nouvelle, la prudence reste de mise. Le monde scientifique sait qu'un cas unique, aussi spectaculaire soit-il, ne constitue pas une preuve statistique suffisante pour valider un traitement pour des millions de personnes. L'enthousiasme légitime suscité par cette réussite doit donc être tempéré par une analyse critique des limites de l'étude. Le patient de Shanghai représente une exception médicale, un « best-case scenario » qui ne reflète peut-être pas la complexité de la population diabétique mondiale.
Il est impératif de comprendre que ce qui fonctionne sur un individu fortement immunodéprimé suite à une greffe de rein pourrait ne pas fonctionner sur une personne en bonne santé par ailleurs. Le corps médical international reste vigilant, attendant que ces résultats soient reproduits sur un échantillon plus large de patients. C'est la démarche scientifique classique : observer, valider, reproduire. Néanmoins, cette percée a le mérite de briser un plafond de verre psychologique, prouvant que la guérison n'est pas une impossibilité biologique.
L'avis du Pr Timothy Kieffer : « une avancée importante »
L'impact de cette étude a dépassé les frontières de la Chine, attirant l'attention des experts mondiaux. Parmi eux, le professeur Timothy Kieffer, de l'Université de la Colombie-Britannique au Canada, a salué ce travail comme « une avancée importante dans le domaine de la thérapie cellulaire pour le diabète ». Son avis est pondéré mais porteur d'espoir : il reconnaît la valeur de la preuve de concept tout en insistant sur la condition sine qua non de toute découverte scientifique, la reproductibilité.
Si d'autres équipes parviennent à obtenir des résultats similaires, les conséquences pourraient être gigantesques. Le Pr Kieffer souligne que cela pourrait « libérer les patients du fardeau des médicaments chroniques, améliorer la santé et la qualité de vie, et réduire les dépenses de santé ». L'enjeu économique est colossal : le diabète est l'une des maladies les plus coûteuses pour les systèmes de santé modernes. Un traitement curatif, même onéreux à court terme, pourrait s'avérer rentable sur le long terme en éradiquant les coûts de gestion des complications (dialyse, cécité, amputations).
L'ombre de l'immunosuppression : un biais méthodologique
Cependant, un biais méthodologique majeur est souligné par plusieurs spécialistes : le patient prenait déjà des immunosuppresseurs pour sa greffe de rein. Ces médicaments servent à calmer le système immunitaire pour qu'il n'attaque pas l'organe étranger, mais ils protègent aussi mécaniquement les nouvelles cellules pancréatiques greffées. Or, dans le cas du diabète de type 2 « classique », les patients ne prennent pas ces médicaments. La question cruciale est : comment protéger ces nouvelles cellules chez un patient dont le système immunitaire est actif ?
Pour le diabète de type 1, la difficulté est encore plus grande car c'est une maladie auto-immune : le système immunitaire attaque spécifiquement les cellules bêta du pancréas. Même si l'on greffe de nouvelles cellules saines, le système immunitaire risque de les détruire à nouveau, comme il l'a fait pour les premières. C'est pourquoi le défi futur n'est pas seulement de fabriquer des cellules, mais aussi de les « camoufler » ou de modifier le système immunitaire pour qu'il les tolère. Le diabète insulinodépendant, c'est quoi exactement ? reste une cible complexe pour ces thérapies, bien que les progrès réalisés sur une patiente de 25 ans à Tianjin offrent aussi des perspectives rassurantes.
Entre espoir et inégalités : un remède à 125 000 dollars ?
Au-delà de la prouesse technique, cette avancée soulève des questions brûlantes d'ordre éthique et économique. La médecine personnalisée, fondée sur la manipulation du génome et des cellules, est par essence extrêmement coûteuse. Le risque est réel de voir apparaître une médecine à deux vitesses : une médecine de luxe, capable de guérir, pour une minorité fortunée, et une médecine de maintenance, traitant seulement les symptômes, pour la grande majorité.
Les sociétés modernes vont devoir se préparer à ce choc. Si le coût de ces thérapies ne baisse pas drastiquement grâce aux progrès industriels, les systèmes de sécurité sociale pourront difficilement les prendre en charge pour tous. Cela pourrait créer des fractures sociales inédites, où l'accès à la guérison deviendrait un marqueur de statut social. Il est urgent de réfléchir aux modèles économiques qui permettront de démocratiser ces innovations, pour que le miracle de Shanghai ne reste pas une anomalie réservée à une élite mondiale.
Le coût exorbitant de la médecine personnalisée
Les estimations concernant le coût des thérapies par cellules souches sont vertigineuses. Selon diverses analyses économiques, un traitement complet peut varier entre 6 000 et 125 000 dollars par patient. Cette fourchette large dépend de la complexité du protocole, du type de cellules utilisées et de la durée de l'hospitalisation. Même en prenant le bas de la fourchette, cela représente une somme considérable comparée au coût annuel des traitements classiques comme la metformine, qui ne coûte que quelques euros par mois.
En France, où environ 4,2 millions de personnes sont traitées pour le diabète, la généralisation d'un tel traitement à 100 000 euros par tête impacterait lourdement le budget de la Sécurité sociale. C'est tout le paradoxe des thérapies géniques et cellulaires : elles promettent d'économiser des milliards à long terme en guérissant les maladies chroniques, mais elles exigent un investissement massif initial. Les décideurs publics vont devoir arbitrer entre cet investissement colossal et l'entretien du système actuel. C'est un calcul complexe qui mêle éthique, économie et santé publique.
L'Europe et la France à la traîne, mais en marche
Il serait faux de croire que l'Occident est à la traîne en matière de recherche sur le diabète. Si la Chine a frappé un grand coup médiatique, l'Europe dispose également de solides pôles d'excellence. En France, par exemple, la greffe d'îlots pancréatiques est devenue une réalité clinique remboursée depuis 2021, mais dans des conditions très strictes. Elle est réservée aux cas graves de diabète de type 1 instable ou aux patients ayant déjà subi une greffe de rein. Des centres experts à Lille, Paris et Montpellier pratiquent déjà ces interventions avec succès.
De plus, des essais cliniques européens sont en cours, menés par des sociétés comme ViaCyte, qui testent des implants de cellules souches différenciées encapsulées pour les protéger du système immunitaire. La différence d'approche réside souvent dans la régulation : l'Europe et la France privilégient une progression plus lente, plus sécurisée, encadrée par des agences de santé strictes comme l'ANSM ou la HAS. Si le rythme est moins médiatique qu'en Chine, il garantit une intégration plus sûre dans le parcours de soins standard, assurant que lorsque la thérapie sera disponible, elle le sera pour tous, dans un cadre médicalisé et contrôlé.
Au-delà de la « pilule miracle » : ce que la jeunesse doit retenir pour sa santé
Cette actualité spectaculaire ne doit pas faire oublier une réalité sanitaire fondamentale : le diabète de type 2 reste une maladie étroitement liée au mode de vie. L'arrivée potentielle d'un remède technologique ne doit pas servir de prétexte à l'inaction individuelle. Pour la génération actuelle de jeunes adultes, âgés de 16 à 25 ans, le message de santé publique est clair : la prévention reste la meilleure stratégie. Attendre un hypothétique remède dans quelques décennies pour prendre soin de soi serait une erreur stratégique dangereuse.
Il est essentiel de rappeler que même si ce traitement de pointe est prometteur, vivre avec un diabète mal contrôlé pendant des années avant de bénéficier d'une greffe laisse des traces irréversibles sur l'organisme. Les complications vasculaires, nerveuses ou rétiniennes ne s'effacent pas toujours comme par magie une fois la glycémie normalisée. C'est pourquoi l'éducation à la santé et à l'hygiène de vie reste le pilier central de la lutte contre cette épidémie moderne, parallèlement aux efforts de recherche génétique.
Ne pas attendre la thérapie cellulaire pour changer de vie
L'alimentation moderne, riche en sucres rapides et en aliments ultra-transformés, couplée à la sédentarité, est le principal moteur de l'épidémie de diabète de type 2. Les jeunes générations sont particulièrement exposées à ces facteurs de risque. L'espoir d'une guérison future ne doit pas inciter à négliger les bases d'une bonne santé : une alimentation équilibrée, une activité physique régulière et un sommeil suffisant. Ce sont ces comportements qui retardent, voire empêchent l'apparition de la maladie.
Il est crucial de comprendre que la thérapie cellulaire n'est pas une « baguette magique » qui permettrait de vivre sans conséquences. Le coût, la complexité et l'accessibilité de ces traitements les réservent, pour les années à venir, à des cas très spécifiques. Pour l'écrasante majorité de la population, la clé de la santé restera la prévention. L'actualité de Shanghai est fascinante, mais elle ne change pas la règle d'or : mieux vaut préserver son pancréas que d'avoir à le reconstruire en laboratoire vingt ans plus tard.
Une lueur d'espoir pour un avenir sans seringue
Malgré ces réserves, il faut saluer ce que cette étude représente : un changement de paradigme. Pendant des décennies, le dogme médical affirmait que le diabète de type 2 était une maladie progressive et irréversible. Ce cas de Shanghai vient briser ce déterminisme. Il prouve qu'il est possible, techniquement et biologiquement, de réparer les dégâts causés par la maladie et de restaurer une fonctionnalité perdue. C'est une lueur d'espoir immense pour tous ceux qui vivent avec cette pathologie au quotidien.
Cette avancée nous projette vers un avenir où la médecine ne se contentera plus de gérer les symptômes chroniques, mais où elle réparera l'humain. La médecine régénérative n'en est qu'à ses débuts, mais ses promesses sont vertigineuses. Entre l'ingénierie tissulaire, la thérapie génique et les cellules souches, nous assistons à l'émergence d'une capacité à soigner que l'on croyait impossible il y a encore quelques années. Si la route vers une « guérison » généralisée est encore longue et semée d'embûches financières et techniques, le cap est désormais tracé. Une génération future pourrait bien voir l'ère des seringues d'insuline comme un chapitre révolu de l'histoire médicale.
Conclusion
L'annonce de la rémission d'un patient diabétique à Shanghai grâce à une thérapie par cellules souches marque une étape historique dans la lutte contre cette maladie. Nous avons vu comment la reprogrammation des propres cellules du sang a permis de recréer un tissu pancréatique fonctionnel, offrant une liberté sans précédent vis-à-vis de l'insuline après 25 ans de maladie. Cependant, cette prouesse technique doit être analysée avec lucidité : elle repose pour l'instant sur un cas unique complexe et reste très coûteuse à mettre en œuvre.
Les défis à relever sont encore immenses. Il faudra prouver la reproductibilité de ces résultats sur un plus grand nombre de patients, résoudre l'équation de l'immunosuppression pour ne pas dépendre d'une greffe d'organe préalable, et surtout rendre ces traitements accessibles financièrement au plus grand nombre. En attendant, cette découverte nous offre une vision fascinante de l'avenir de la médecine et rappelle l'importance cruciale de la recherche, tout en nous laissant une responsabilité individuelle : celle de protéger notre santé aujourd'hui pour ne pas avoir à dépendre de ces solutions miracles demain.