L'histoire de la médecine est parfois jalonnée de chiffres qui semblent défier le hasard et réécrire les possibles. Récemment, une publication parue dans le Journal of Clinical Investigation par l'équipe de l'Université de Stanford a fait l'effet d'une bombe dans le monde de l'endocrinologie. Les résultats rapportés sont d'une précision chirurgicale : 19 souris sur 19 ont été protégées du développement du diabète, et 9 souris sur 9, déjà malades, ont été guéries. Mais au-delà de ces statistiques parfaites, c'est la nature même de l'étude qui marque une rupture fondamentale avec les tentatives précédentes.
Pour la première fois, des chercheurs sont parvenus à inverser le cours d'un diabète de type 1 auto-immun chez l'animal, et non un diabète provoqué artificiellement par une toxine. Cette distinction est cruciale car elle mime la pathologie humaine, où le système immunitaire tourne ses armes contre ses propres cellules pancréatiques. Pour les millions de personnes qui doivent mesurer chaque gramme de glucides et piquer leur insuline plusieurs fois par jour, cette étude redéfinit les frontières de l'espoir. Elle ouvre la voie à une guérison potentielle qui ne nécessiterait plus de détruire le système immunitaire du patient pour le reconstruire, une perspective inédite jusque-là.

Quand 28 souris deviennent le symbole d'un espoir immense
L'expérience réalisée à Stanford ne relève pas de la simple expérimentation de laboratoire ; elle est une démonstration de force conceptuelle. En utilisant des souris NOD (Non-Obese Diabetic), les chercheurs ont travaillé avec un modèle animal qui développe spontanément un diabète auto-immun extrêmement similaire à celui qui touche les humains. Ces souris ne sont pas rendues malades par une injection chimique, elles « attrapent » naturellement la maladie, exactement comme un adolescent peut développer un diabète de type 1 sans raison apparente. C'est ce qui rend la réussite de l'équipe de Seung K. Kim si pertinente pour notre propre biologie.
La signification de ces 28 souris ne se mesure pas à l'aune de leur petit nombre, mais à la lumière de ce qu'elles représentent pour l'avenir thérapeutique. Chaque souris guérie est la preuve vivante que la barrière de l'auto-immunité peut être franchie sans utiliser les méthodes brutales du passé. C'est la promesse qu'un jour, le traitement du diabète de type 1 ne sera plus une gestion quotidienne pénible, mais une intervention unique capable de restaurer l'équilibre physiologique naturel. L'émotion que suscitent ces résultats réside dans cette possibilité concrète de se libérer d'une maladie chronique qui, jusqu'à présent, accompagnait ses victimes toute leur vie.
19 souris sur 19, 9 souris sur 9 : des chiffres qui défient l'imaginaire
Dans le domaine de la recherche biomédicale, obtenir un taux de succès de 100 % est aussi rare qu'exceptionnel. L'étude de Stanford présente deux groupes de souris qui racontent deux facettes de la même victoire. Le premier groupe comprenait 19 souris pré-diabétiques, c'est-à-dire dont le système immunitaire commençait tout juste à s'agiter mais qui n'avait pas encore besoin d'insuline pour survivre. Après le protocole expérimental, ces 19 souris ont vécu une vie normale, sans jamais développer la maladie, comme si leur système immunitaire avait été « réinitialisé » à temps.
Le deuxième groupe, encore plus impressionnant, était composé de 9 souris déjà atteintes de diabète avancé et dépendantes de l'insuline pour maintenir une glycémie vitale. Après le traitement, ces 9 souris ont vu leur glycémie se normaliser durablement et ont pu cesser toute injection d'insuline. Le fait que l'intégralité de ce groupe secondaire ait été guérie suggère que la méthode fonctionne aussi bien en prévention qu'en traitement curatif. Cette constance dans les résultats, de la prévention à la rémission totale, démontre une robustesse du protocole rarement observée dans les essais précliniques.
Pourquoi cette étude n'est PAS une de plus parmi tant d'autres
Il est facile de se perdre dans le flot constant d'annonces scientifiques prometteuses qui finissent par s'éteindre dans l'indifférence. Pourtant, l'étude de Stanford se distingue radicalement de la majorité des travaux précédents sur le diabète. Historiquement, la majorité des « guérisons » chez l'animal étaient obtenues sur des modèles de diabète de type 1 induit chimiquement, souvent par la streptozotocine, une substance toxique qui détruit directement les cellules bêta du pancréas. Dans ces cas, le problème est purement mécanique : les cellules sont mortes, il faut en remplacer. C'est difficile, mais conceptuellement simple.
Le véritable défi du diabète de type 1 humain est l'aspect auto-immun : même si l'on greffe de nouvelles cellules productrices d'insuline, le système immunitaire du patient les traite comme des envahisseurs et les détruit immédiatement. C'est comme tenter de repeindre un mur en feu : tant que l'incendie fait rage, la peinture ne tiendra pas. En réussissant à stopper l'attaque auto-immune chez des souris NOD, l'équipe de Stanford a éteint l'incendie avant de reconstruire la maison. C'est cette double prouesse — arrêter la maladie auto-immune et restaurer la fonction insulinique — qui classe cette étude dans une catégorie à part.
Le pari fou de Seung K. Kim : greffer sans détruire le système immunitaire
Au cœur de cette révolution se trouve le professeur Seung K. Kim et son équipe de la Stanford Medical School. Leur pari semblait, à première vue, contradictoire avec les dogmes établis de la transplantation. Pendant des décennies, la règle d'or pour accepter une greffe d'organe ou de cellules étrangères était de réduire au silence le système immunitaire du receveur. Cela se traduisait par une chimiothérapie lourde, souvent myéloablative, c'est-à-dire une irradiation massive visant à détruire la moelle osseuse et le système immunitaire existant pour le remplacer par celui du donneur. C'est une procédure extrêmement risquée, lourde de complications immédiates et à long terme.
L'équipe de Kim a choisi une voie radicalement différente, celle de la « greffe douce ». Inspirée par les travaux pionniers de chercheurs comme Samuel Strober et Judith Shizuru à Stanford, qui avaient démontré la faisabilité de greffes de rein sans immunosuppresseurs à vie grâce à des techniques d'induction de tolérance, l'équipe a adapté ces concepts au pancréas. L'idée n'est pas de bombarder le corps avec des produits chimiques mortels, mais de le convaincre, par des interventions ciblées et douces, d'accepter les nouveaux venus comme ses propres enfants. C'est une approche qui privilégie la persuasion biologique à la force brute.
Stanford, novembre 2025 : la publication qui change tout
La parution de l'étude dans le Journal of Clinical Investigation en novembre 2025 n'est pas arrivée par hasard. Elle est le fruit d'une longue maturation scientifique qui trouve ses racines dans une publication antérieure de la même équipe, en novembre 2022, dans la revue Cell Reports. À l'époque, les chercheurs avaient déjà réussi à guérir des souris atteintes de diabète induit, en utilisant une combinaison de radiothérapie à faible dose et d'anticorps ciblés. Cependant, le passage au diabète auto-immun, le « Graal » de la recherche dans ce domaine, restait à conquérir.
Ce qui a changé en 2025, c'est l'affinement du protocole de conditionnement. L'équipe a perfectionné la recette pour qu'elle fonctionne sur un système immunitaire véritablement hostile et actif, comme c'est le cas chez les souris NOD et chez les humains atteints de diabète de type 1. La publication ne fait pas seulement état de résultats ; elle décrit une méthodologie reproductible et rigoureuse qui a survécu à l'examen critique des pairs scientifiques. En validant cette approche sur un modèle auto-immun, Stanford a transformé une curiosité de laboratoire en une piste thérapeutique crédible.
De la chimiothérapie lourde aux quatre composants doux
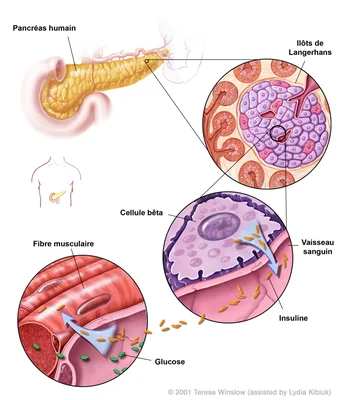
Le secret de cette réussite réside dans un cocktail de quatre composants administrés avant la greffe, conçus pour préparer l'accueil sans détruire l'hôte. Contrairement aux traitements classiques qui laissent le patient immunodéprimé pendant des mois, ce conditionnement « non-myéloablatif » est beaucoup moins agressif. Le premier élément est un anticorps anti-CD117. Le CD117 est un marqueur présent à la surface des cellules souches sanguines ; en le ciblant, l'anticorps permet de vider les « niches » de la moelle osseuse pour faire de la place aux nouvelles cellules du donneur, sans irradier le corps entier de manière destructrice.
Le deuxième composant est un inhibiteur JAK1/2, une classe de médicaments déjà utilisée en clinique humaine pour traiter des maladies inflammatoires ou certaines myélofibroses. Ce médicament calme temporairement l'activité du système immunitaire, réduisant l'inflammation et l'hostilité générale sans l'éteindre complètement. Le troisième élément est une dose d'anticorps anti-cellules T matures, qui retire de la circulation les soldats les plus agressifs du système immunitaire qui pourraient attaquer la greffe immédiatement. Enfin, une radiothérapie à très faible dose est utilisée, non pour détruire, mais pour affaiblir suffisamment les défenses locales pour permettre l'installation des cellules souches.
L'astuce du chimérisme : un système immunitaire à deux têtes
La compréhension de la réussite de cette étude repose sur un concept biologique fascinant : le chimérisme hématopoïétique. Le terme vient de la Chimère, cette créature mythique composée de parties de différents animaux. En biologie, un chimérisme hématopoïétique désigne un état où le système sanguin d'un individu contient un mélange de ses propres cellules souches et de celles d'un donneur. C'est un peu comme si deux systèmes d'exploitation tournaient en parallèle sur le même ordinateur, en parfaite harmonie.
Dans l'étude de Stanford, la greffe de cellules souches sanguines du donneur ne sert pas seulement à remplacer les cellules défectueuses ; elle sert à « rééduquer » le système immunitaire du receveur. En créant ce système hybride, les cellules immunitaires issues des cellules souches du donneur apprennent aux cellules du receveur que les îlots pancréatiques greffés sont « soi » et non « non-soi ». C'est une diplomatie cellulaire qui permet de créer un climat de tolérance permanent. Une fois que ce système immunitaire hybride est en place, il protège la greffe contre toute attaque, y compris celle qui proviendrait des propres cellules restées du receveur.
Cellules souches sanguines + îlots pancréatiques : l'équation gagnante
L'innovation majeure de cette étude réside dans la combinaison de deux types de greffons provenant du même donneur. Il ne suffit pas de greffer les îlots pancréatiques, ces petites îles de cellules productrices d'insuline ; il faut aussi greffer le « garde du corps » qui les protégera. Les cellules souches sanguines, une fois transplantées et installées dans la moelle osseuse du receveur, vont générer tout le système immunitaire futur qui reconnaîtra comme « amis » à la fois le receveur et les îlots greffés.
Cette équation fonctionne comme une serrure et sa clé. Les îlots sont la clé qui permet de régler le sucre, mais sans la serrure (la tolérance immunitaire apportée par les cellules souches), la clé ne peut pas tourner. Dans les protocoles précédents, on essayait de changer la serrure (le patient) pour qu'elle accepte la clé. Ici, on change une partie du mécanisme interne pour que la serrure s'adapte naturellement à la clé fournie. C'est pourquoi la compatibilité entre les cellules souches et les îlots est absolument critique : ils doivent être issus du même donneur pour que les cellules immunitaires produites par les premières acceptent les seconds comme leur propre corps.
Comment le système immunitaire se fait « rééduquer » sans violence
Le processus de tolérance mis en évidence dans cette étude est un véritable tour de force biologique. Une fois les cellules souches sanguines du donneur installées dans la moelle du receveur, elles commencent à produire des lymphocytes T et B qui portent les marqueurs du donneur. Ces nouvelles cellules immunitaires vont circuler dans le corps et patrouiller. Lorsqu'elles rencontrent les îlots pancréatiques greffés, qui portent les mêmes marqueurs qu'elles, elles ne déclenchent pas d'attaque. Au contraire, elles les intègrent à leur « liste des amis ».
Ce qui est remarquable, c'est l'effet domino sur les cellules immunitaires résiduelles du receveur, celles qui n'ont pas été détruites par le conditionnement doux. La présence des cellules du donneur crée un environnement régulateur qui calme l'agressivité des cellules auto-immunes restantes. C'est un phénomène d'éducation par la cohabitation : en vivant ensemble, les deux populations cellulaires apprennent la tolérance mutuelle. Le système immunitaire devient ainsi un « système à deux têtes », capable de défendre l'organisme contre les infections réelles, mais aveugle aux îlots pancréatiques.
Ce qui se cache entre les lignes de l'euphorie scientifique
Malgré l'enthousiasme justifié suscité par ces résultats, la communauté scientifique reste lucide. La recherche médicale est un marathon semé d'embûches, et chaque avancée majeure s'accompagne de son lot de défis logistiques et biologiques. L'équipe de Stanford elle-même souligne plusieurs obstacles majeurs qui doivent être surmontés avant que cette thérapie puisse être proposée aux patients humains. Il est essentiel de comprendre ces limites non pour minimiser la découverte, mais pour apprécier la complexité du chemin qui reste à parcourir.
Ces défis ne sont pas insurmontables, mais ils nécessitent des solutions d'ingénierie et des approvisionnements médicaux précis. Ils nous rappellent que ce qui fonctionne parfaitement chez une souris de quelques grammes dans un environnement stérile de laboratoire peut devenir d'une complexité vertigineuse lorsqu'il s'agit de traiter un être humain de 70 kilogrammes. Cette honnêteté intellectuelle est d'ailleurs ce qui rend l'étude si crédible : elle ne cache pas les difficultés, elle les identifie pour qu'elles puissent être résolues.
Le problème des îlots : un donneur décédé pour chaque patient
Le premier obstacle, et non des moindres, est la source des cellules bêta productrices d'insuline. Contrairement aux cellules souches sanguines qui peuvent potentiellement être multipliées en culture ou prélevées chez le donneur vivant, les îlots pancréatiques sont une ressource limitée et fragile. Actuellement, la seule source fiable d'îlots pancréatiques humains fonctionnels pour transplantation est le pancréas de donneurs décédés.
Cela pose un problème de santé publique d'envergure. Si chaque patient diabétique devait recevoir les îlots d'un donneur décédé unique, la demande dépasserait de loin l'offre disponible. On se retrouverait rapidement confronté à la même pénurie que celle observée pour les greffes de rein ou de cœur. De plus, les îlots sont extrêmement sensibles : ils doivent être prélevés, purifiés et transplantés très rapidement pour rester viables. C'est une course contre la montre logistique qui limite la capacité de mise à l'échelle de cette approche.
La contrainte de compatibilité : un seul donneur pour deux greffons
Le deuxième défi majeur est lié à la nécessité d'une double compatibilité. Puisque la méthode repose sur la création d'un chimérisme où les cellules souches du donneur « éduquent » le système immunitaire pour accepter les îlots, il est impératif que les cellules souches et les îlots proviennent du même donneur. On ne peut pas prendre des cellules souches d'une banque et des îlots d'un autre donneur en espérant que cela fonctionnera. Les marqueurs biologiques doivent correspondre parfaitement pour que la tolérance s'établisse.
Cela complique considérablement la chaîne d'approvisionnement. Il ne suffit pas de trouver un donneur d'îlots ; il faut trouver un donneur capable de fournir des cellules souches hématopoïétiques (souvent issues de la moelle osseuse ou du sang circulant) et des îlots pancréatiques en quantité suffisante. Bien que ces deux types de tissus puissent techniquement provenir du même cadavre, la coordination des prélèvements et la gestion des délais sont un casse-tête logistique. C'est un peu comme essayer de trouver deux pièces spécifiques d'un moteur ancien : elles doivent être issues du même modèle exact pour fonctionner ensemble.
De la souris NOD à l'adolescent français : combien d'années devant nous ?
Le passage de l'animal à l'homme, souvent appelé « transfert clinique », est le goulet d'étranglement où de nombreuses thérapies prometteuses ont échoué. Cependant, l'étude de Stanford présente un avantage stratégique indéniable : elle n'invente pas de molécules exotiques ou dangereuses. Les briques élémentaires du protocole sont déjà utilisées en clinique pour d'autres pathologies, ce qui suggère que la sécurité de base de ces composants est déjà connue.
Cela signifie qu'on pourrait potentiellement économiser plusieurs années de tests de toxicité initiaux. Toutefois, la prudence reste de mise. Le passage de la souris NOD à l'humain ne se résume pas à une simple multiplication de la dose par le rapport de poids. Les systèmes immunitaires humains sont plus complexes, ont une mémoire immunologique plus longue et sont exposés à un environnement viral et bactérien beaucoup plus varié que celui des souris de laboratoire. Le professeur Seung K. Kim a d'ailleurs souligné avec optimisme que la possibilité de transposer ces résultats chez l'homme est très excitante, précisément parce que les étapes clés menant à un système immunitaire hybride sont déjà employées cliniquement pour d'autres conditions.
La citation optimiste de Seung K. Kim
L'analyse des propos du professeur Kim révèle une stratégie intelligente : au lieu d'inventer une nouvelle technologie à partir de zéro, Stanford a réassemblé des blocs connus dans une configuration inédite. C'est ce qu'on appelle l'innovation de procédé. Pour les patients, cela signifie que si les essais cliniques confirment l'efficacité chez l'homme, la mise en place de la thérapie dans les hôpitaux pourrait se faire plus rapidement que pour des médicaments entièrement nouveaux, car les équipes médicales connaissent déjà la manipulation et la gestion de ces produits thérapeutiques.
Essais cliniques : le long chemin qui reste à parcourir
Malgré cet optimisme, il est crucial de rappeler que le chemin entre la souris et la pilule est long. Les essais cliniques se déroulent généralement en trois phases. La phase I teste la sécurité sur un petit groupe de volontaires sains ou de patients gravement atteints. La phase II évalue l'efficacité et détermine la dose optimale. La phase III est un essai à grande échelle pour confirmer l'efficacité et surveiller les effets secondaires rares. Ce processus prend souvent plusieurs années, parfois une décennie.
De plus, les dosages chez l'homme posent des questions complexes. Une souris pèse environ 20 à 30 grammes, contre 70 kilogrammes pour un humain. La surface corporelle, le métabolisme et le volume sanguin ne suivent pas une simple règle de trois. Les chercheurs devront déterminer avec précision quelle quantité d'anticorps et de cellules souches est nécessaire pour induire le chimérisme sans provoquer de toxicité. C'est un équilibre délicat, comme ajuster la sensibilité d'une balance : trop faible, la greffe est rejetée ; trop fort, le risque de complication devient inacceptable.
La Chine, Stanford, et la course mondiale aux cellules souches
L'actualité scientifique récente nous montre que la recherche sur le diabète de type 1 est plus dynamique que jamais, et que des solutions différentes émergent aux quatre coins du globe. Alors que l'approche de Stanford se concentre sur la tolérance immunitaire via un donneur extérieur, une équipe chinoise de l'Université de Nankai a publié, en octobre 2024, des résultats tout aussi spectaculaires mais avec une philosophie diamétralement opposée. Ils ont réussi à « guérir » une femme de 25 ans en utilisant ses propres cellules, ce qui évite complètement le problème du rejet.
Ces deux avancées, bien que différentes, ne sont pas concurrentes mais complémentaires. Elles montrent qu'il n'y a pas une seule route vers la guérison, mais plusieurs chemins convergents. D'un côté, l'approche américaine utilise une « greffe douce » allogénique (d'un autre individu) pour rééduquer le système immunitaire. De l'autre, l'approche chinoise utilise une autogreffe (cellules du patient) pour créer de nouvelles cellules productrices d'insuline. Ensemble, elles dessinent la carte d'un monde médical où le diabète de type 1 pourrait enfin devenir une maladie du passé.
Octobre 2024, Chine : une femme de 25 ans guérie par ses propres cellules
L'histoire rapportée par Le Monde en octobre 2024 marque une étape décisive. Une équipe de l'université de Nankai est parvenue à traiter une patiente de 25 ans atteinte de diabète de type 1 depuis 11 ans. La méthode utilisée est fascinante : au lieu de faire appel à un donneur externe, les chercheurs ont prélevé du tissu adipeux (de la graisse) sur la patiente elle-même. À partir de ces cellules souches adipiques, ils ont cultivé in vitro des cellules productrices d'insuline.
L'intervention a été d'une simplicité déconcertante : une simple injection dans les muscles de l'abdomen, réalisée en moins de 30 minutes. Les résultats ont été jugés « spectaculaires » par François Pattou, chirurgien au CHU de Lille et spécialiste reconnu du domaine. La patiente a pu se passer d'insuline, son corps régulant à nouveau son taux de sucre naturellement. Ici, la force de la méthode réside dans l'autonomie : on utilise le corps comme usine à médicaments.
Deux approches, un même objectif : comparer sans opposer
Il est tentant de vouloir opposer ces deux découvertes pour savoir laquelle est la « meilleure ». En réalité, elles répondent à des problématiques différentes et pourraient servir des types de patients différents. L'approche Stanford nécessite un donneur externe (avec les problèmes de pénurie que cela implique) mais offre l'avantage théorique de « rééduquer » le système immunitaire pour qu'il arrête toute attaque auto-immune. L'approche chinoise utilise les cellules du patient (pas de problème de donneur) mais repose sur l'hypothèse que l'environnement immunitaire ne détruira pas les nouvelles cellules.
On peut imaginer que dans le futur, les approches pourraient converger. Peut-être qu'un jour, on prendra les cellules souches d'un patient (comme à Nankai), on les modifiera génétiquement (en utilisant des techniques comme la thérapie génique) pour les rendre invisibles au système immunitaire, puis on les greffera selon un protocole doux inspiré de celui de Stanford. Ce sont les briques d'un puzzle immense que les chercheurs du monde entier assemblent ensemble, brique après brique. D'autres pistes, comme celles explorées pour le diabète de type 2 à Shanghai, montrent que le champ des possibles s'élargit rapidement.
Vivre avec le diabète de type 1 aujourd'hui, en attendant demain
Au milieu de ces avancées scientifiques vertigineuses, il ne faut jamais perdre de vue la réalité quotidienne des millions de personnes vivant avec le diabète de type 1 aujourd'hui. Pour un adolescent qui reçoit son diagnostic, ou pour un parent qui doit gérer la maladie de son enfant, l'espoir d'une guérison ne doit jamais faire oublier la lourdeur du présent. Vivre avec le diabète de type 1, c'est gérer une entreprise complexe 24 heures sur 24, 7 jours sur 7, sans jamais pouvoir prendre de congé.
Cette maladie est une charge mentale invisible mais constante. Chaque repas devient un exercice de mathématiques : peser les aliments, estimer les glucides, calculer la dose d'insuline en tenant compte de l'activité physique prévue, de la glycémie actuelle, de la sensibilité individuelle, et même du stress ou de la météo. C'est un équilibre précaire où une erreur de calcul ou une surprise imprévue peut entraîner une hypoglycémie dangereuse ou une hyperglycémie toxique sur le long terme.

Une charge mentale invisible mais constante
Imaginez devoir piloter un avion sans jamais pouvoir lâcher les commandes. C'est la métaphore souvent utilisée par les diabétologues pour décrire la gestion du diabète de type 1. Le matin au réveil, la première pensée n'est pas « que vais-je faire aujourd'hui ? » mais « quelle est ma glycémie ? ». Une glycémie trop basse demande un apport de sucre immédiat pour éviter le malaise ; une glycémie trop élevée au réveil gâche souvent l'humeur et l'énergie pour la matinée.
Pendant la journée, le sport n'est pas seulement une question de santé ou de plaisir, c'est un risque calculé. L'effort physique fait chuter la glycémie, il faut anticiper, manger des collations, parfois baisser les doses d'insuline avant l'entraînement. La nuit, la peur de l'hypoglycémie sévère (le « coma ») peut empêcher les parents de dormir, ou le patient lui-même de se reposer complètement. Des appareils de mesure en continu et des pompes à insuline automatisées ont grandement amélioré la qualité de vie, mais ils ne libèrent pas le patient de la nécessité de surveiller les chiffres et de prendre des décisions thérapeutiques constantes.
Ce que promet vraiment la « greffe douce » : une vie libérée
C'est pourquoi les recherches de Stanford et de Nankai sont si importantes. Elles ne promettent pas seulement une amélioration de la prise en charge médicale ; elles promettent une libération existentielle. Imaginez un instant ce que signifie pour un jeune diabétique l'idée d'une « greffe douce » réussie. Se réveiller le matin sans avoir à se piquer le doigt. Prendre son petit-déjeuner sans avoir à peser ses céréales ou compter les glucides de son fruit. Aller courir avec des amis sans avoir une friandise dans la poche au cas où la glycémie chuterait brutalement.
Cette promesse d'une vie libérée de la charge mentale et du poids de la maladie est ce qui motive les chercheurs, et c'est ce qui doit nous guider dans notre compréhension de ces avancées. Ce n'est pas seulement une question de chimie sanguine ou de biologie cellulaire, c'est une question de liberté retrouvée. La guérison promise par ces études n'est pas un rêve abstrait de scientifique enfermé dans son labo ; c'est l'espoir concret de millions de personnes de pouvoir vivre leur vie sans que leur maladie ne soit le personnage principal de chaque journée.
Conclusion : 2025, l'année où l'« impossible » a commencé à trembler
L'année 2025 restera peut-être dans les annales de l'histoire médicale comme celle où le mur de l'« impossible » face au diabète de type 1 a commencé à sérieusement trembler. Avec l'annonce de l'étude de Stanford en novembre, venant après les résultats chinois de 2024, nous avons assisté à une accélération brutale des connaissances. La démonstration qu'une greffe douce, épargnant le système immunitaire, peut guérir un diabète auto-immun chez la souris est une avancée conceptuelle majeure. Le concept de chimérisme hématopoïétique, transformant le système immunitaire ennemi en allié, ouvre des perspectives inédites pour le traitement de nombreuses autres maladies auto-immunes.
Cependant, comme nous l'avons vu, le chemin est encore long. Les défis logistiques des îlots pancréatiques, la contrainte de la compatibilité donneur-receveur et les étapes obligatoires des essais cliniques nous rappellent qu'il faut rester prudents. La science ne fonctionne pas par miracle, mais par rigueur. Néanmoins, l'atmosphère a changé. Pour la génération de jeunes diabétiques d'aujourd'hui, la question n'est plus désespérément « si » un jour le diabète pourra être guéri, mais « quand » ces protocoles seront disponibles à l'hôpital. C'est un changement de perspective immense, porté par la science et la détermination de chercheurs comme ceux de Stanford. Le temps de la gestion acharnée n'est pas encore fini, mais le temps de la guérison s'approche à grands pas.