Lundi 23 février 2026, le monde financier et médical a retenu son souffle. L'annonce de l'acquisition d'Arcellx par le géant californien Gilead Sciences pour une somme potentielle de 7,8 milliards de dollars a fait l'effet d'une bombe. Bien plus qu'une simple transaction boursière, ce mouvement marque une accélération brutale dans la course aux thérapies cellulaires, ces traitements révolutionnaires qui redéfinissent les espoirs de guérison contre le cancer. Alors que les laboratoires se livrent une bataille sans merci pour sécuriser les technologies les plus prometteuses, cette acquisition soulève des questions cruciales sur l'avenir de notre santé, le coût de l'innovation et l'accessibilité de ces « miracles » biologiques pour les patients.

7,8 milliards de dollars : quand Gilead paie une prime record pour l'avenir du myélome
En offrant près de huit milliards de dollars pour racheter une entreprise dont le produit phare n'a pas encore été officiellement commercialisé, Gilead envoie un signal puissant aux marchés financiers et à ses concurrents. Cette somme vertigineuse ne reflète pas seulement la valeur actuelle d'Arcellx, mais surtout l'anticipation d'un marché colossal pour les traitements contre le myélome multiple, un cancer du sang encore difficile à soigner à un stade avancé. C'est un investissement massif qui vise à compenser le déclin inévitable des revenus liés à la pandémie, notamment ceux du Veklury, l'antiviral star de Gilead contre le COVID-19, dont les ventes s'essoufflent.

L'opération du 23 février 2026 : une prime de 79% pour convaincre Arcellx
Les détails de l'opération, conclus le lundi 23 février 2026, démontrent à quel point Gilead voulait verrouiller ce dossier à tout prix. L'accord prévoit le paiement de 115 dollars en espèces par action, assorti d'un « contingent value right » (CVR) de 5 dollars supplémentaires. Ce mécanisme financier ingénieux permet aux actionnaires d'Arcellx de toucher une prime supplémentaire si les ventes futures de la star du laboratoire, l'anito-cel, atteignent le seuil symbolique des 6 milliards de dollars. Au total, cette valorisation représente une prime de 79% par rapport au cours de clôture de l'action Arcellx avant l'annonce, une offre difficile à refuser pour les actionnaires de la biotechnologie.
Une telle prime révèle l'urgence de la situation pour Gilead. En payant presque le double de la valeur de marché de l'entreprise cible, le laboratoire américain s'assure qu'aucun autre concurrent ne puisse venir perturber l'opération au dernier moment. C'est la plus importante acquisition menée par Gilead depuis son rachat d'Immunomedics en 2020 pour 21 milliards de dollars, un pari qui s'était déjà révélé payant dans le secteur de l'oncologie. Cette stratégie d'acquisition agressive permet à Gilead de maintenir sa croissance malgré l'arrivée prochaine de la fin de certains brevets historiques, qui menacent ses revenus dans les années à venir. L'opération devrait être finalisée au cours du deuxième trimestre 2026.
Plus qu'une entreprise, l'achat d'un portefeuille : pourquoi Arcellx ?
Au-delà des bâtiments et des équipes de recherche, ce que Gilead a réellement acheté pour 7,8 milliards de dollars, c'est une plateforme technologique de pointe. Arcellx n'est pas une entreprise pharmaceutique classique avec un portefeuille de médicaments déjà sur le marché ; c'est une pépite biotechnologique qui a développé une méthode unique pour manipuler le système immunitaire. Le joyau de la couronne est sans conteste l'anito-cel, une thérapie cellulaire expérimentale qui pourrait devenir le nouveau standard de soins pour le myélome multiple.

Cette acquisition s'inscrit dans une logique de remplissage du pipeline, terme qui désigne l'ensemble des médicaments en cours de développement. Pour une firme pharmaceutique, il est crucial de continuellement renouveler ce catalogue de futurs produits. Comme le souligne l'analyse du cancer de la mondialisation bancaire et économique, les stratégies des géants de la santé doivent s'adapter aux incertitudes globales. Gilead se devait donc de trouver une nouvelle locomotive de croissance, et Arcellx, avec sa technologie propriétaire « domaine D », offre exactement cela : une porte d'entrée vers un marché où la demande est forte et l'offre médicale encore insuffisante.
Une stratégie pour contrer l'érosion des revenus historiques
Gilead Sciences est un groupe habitué à gérer des « blockbusters », mais ces dernières années, le contexte a changé. Le laboratoire a bâti sa fortune sur les antiviraux, notamment dans le traitement du VIH et des hépatites, et plus récemment avec le remdesivir pendant la crise sanitaire. Cependant, la fin de l'état d'urgence sanitaire et la concurrence accrue sur les traitements antiviraux ont créé un vide financier qu'il est impératif de combler rapidement.
L'acquisition d'Arcellx permet à Gilead de pivoter stratégiquement vers l'oncologie hématologique, un secteur en pleine expansion et moins sujet aux cycles épidémiques. En sécurisant l'anito-cel, le laboratoire diversifie ses sources de revenus et réduit sa dépendance aux traitements contre les maladies infectieuses. C'est une mue nécessaire pour un géant pharmaceutique qui doit prouver à ses actionnaires qu'il peut générer de la croissance organique même sans pandémie mondiale. L'opération marque donc le point de départ de cette nouvelle orientation stratégique, plaçant l'oncologie au cœur de son futur modèle économique.
Anito-cel : transformer les cellules du patient en armes biologiques intelligentes
Une fois le choc financier passé, il est essentiel de comprendre ce que cet investissement massif va concrètement apporter à la médecine. L'anito-cel n'est pas un médicament que l'on prend sous forme de pilule ou d'injection classique. Il s'agit d'une thérapie CAR-T (Chimeric Antigen Receptor T-cell), une technologie au cœur de la médecine de précision qui consiste à prélever les propres cellules immunitaires du patient pour les transformer en de véritables soldats capables de traquer et de détruire le cancer. C'est cette promesse scientifique, à la frontière de la science-fiction et de la biologie, qui justifie le montant colossal déboursé par Gilead.
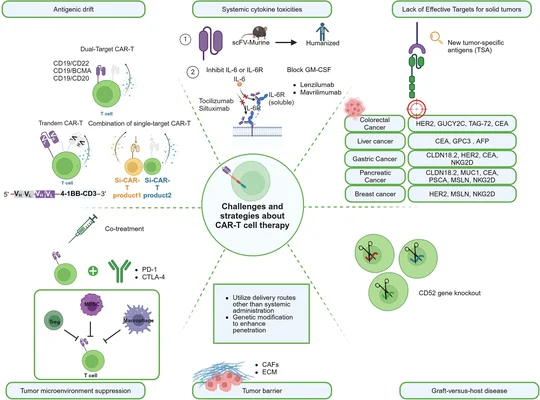
Le fonctionnement « sur-mesure » des thérapies CAR-T
Pour comprendre la révolution apportée par l'anito-cel, il faut imaginer un processus complexe qui débute dans le corps du patient et passe par les laboratoires. Des lymphocytes T, ces cellules blanches qui sont les « commandos » de notre système immunitaire, sont prélevés par prélèvement sanguin. Une fois au laboratoire, ces cellules sont génétiquement modifiées pour exprimer un récepteur chimérique, le fameux CAR, qui agit comme un radar ultra-perfectionné.
Une fois réinjectées dans le corps du patient, ces cellules T modifiées sont capables de cibler spécifiquement l'antigène BCMA (B-cell maturation antigen), une protéine présente à la surface des cellules cancéreuses du myélome multiple. C'est un peu comme si l'on équipait des soldats de jumelles de vision nocturne et de GPS pour qu'ils retrouvent et éliminent uniquement les ennemis cachés au milieu d'une population innocente. Ce traitement « sur-mesure » utilise le corps du patient comme usine de production d'armes biologiques intelligentes, offrant une précision que la chimiothérapie classique, qui s'attaque aux cellules saines et cancéreuses indifféremment, ne pourra jamais égaler.
Des chiffres de survie qui justifient l'investissement : l'étude iMMagine-1
Cependant, une technologie aussi prometteuse doit prouver son efficacité clinique pour justifier un investissement de 7,8 milliards de dollars. Heureusement pour Gilead, les données de l'étude clinique iMMagine-1 concernant l'anito-cel sont rien moins que spectaculaires. Les résultats présentés montrent un taux de réponse globale de 96%, ce qui signifie que sur 117 patients traités, 112 ont vu leur cancer régresser de manière significative.
Plus impressionnant encore, 74% des patients ont atteint une rémission complète ou stringente, un niveau de réponse souvent synonyme de prolongation substantielle de la vie. À l'heure actuelle, la survie sans progression de la maladie est de 82,1% à 12 mois et reste élevée à 61,7% à 24 mois. Ces chiffres sont cruciaux car ils démontrent que l'effet du traitement n'est pas seulement éphémère mais durable dans le temps. C'est sur la base de ces résultats médicaux solides que Gilead a pu convaincre ses investisseurs que l'anito-cel deviendrait un « blockbuster », un terme de l'industrie pour désigner un médicament générant plus d'un milliard de dollars de revenus annuels.
L'avantage technologique du « domaine D » face aux neurotoxicités
L'innovation d'Arcellx ne réside pas uniquement dans l'efficacité, mais aussi dans la sécurité de sa plateforme technologique. Les thérapies CAR-T de première génération souffrent parfois d'un effet secondaire redoutable : la neurotoxicité, qui peut causer des troubles neurologiques sévères chez les patients. Pour remédier à cela, Arcellx a développé une technologie unique basée sur ce qu'ils appellent le « domaine D ». Contrairement aux fragments d'anticorps monoclonaux (scFv) traditionnels utilisés par les concurrents, ces domaines de liaison à la cible propriétaires offrent une meilleure affinité et une spécificité supérieure.
Le résultat le plus marquant observé lors des essais cliniques est l'absence totale de neurotoxicité retardée. Dans le traitement de cancers du sang aussi agressifs que le myélome multiple, pouvoir offrir une efficacité thérapeutique maximale sans risquer d'endommager le système nerveux du patient constitue un avantage concurrentiel majeur. C'est cette spécificité qui pourrait permettre à l'anito-cel de se démarquer face à des traitements déjà existants, en rassurant les autorités de santé et, surtout, les patients terrifiés par les effets secondaires potentiels des traitements agressifs.

La course contre la montre : Gilead face au géant Johnson & Johnson
L'acquisition d'Arcellx ne doit pas être analysée isolément, mais dans le contexte d'une guerre économique féroce qui oppose les géants mondiaux de la santé sur le créneau lucratif de l'oncologie hématologique. Si Gilead a mis la main au portefeuille pour une telle somme, c'est parce qu'il est en retard sur un marché déjà dominé par un tandem redoutable : Johnson & Johnson et son partenaire chinois Legend Biotech. Cette acquisition est donc une réponse stratégique d'urgence pour ne pas laisser une part de marché colossale échapper définitivement à l'américain.
Carvykti, le rival de 1,9 milliard de dollars qui motive tout
L'ombre qui plane sur ce rachat s'appelle Carvykti. Développé par Johnson & Johnson et Legend Biotech, ce traitement concurrent est déjà le leader incontesté du marché des thérapies CAR-T contre le myélome multiple. En 2025 seulement, Carvykti a généré environ 1,9 milliard de dollars de ventes, prouvant qu'il existe une demande solvable et massive pour ces thérapies innovantes. Ce chiffre d'affaires colossal sert de référence aux analystes pour estimer le potentiel d'anito-cel.
Gilead ne cherche pas ici à créer un marché de toutes pièces, mais à damer le pion à un rival déjà installé. L'espoir du laboratoire est que l'anito-cel, grâce à son profil de sécurité supérieur et à ses données cliniques encourageantes, puisse grignoter les parts de marché de Carvykti. Selon Brian Abrahams, analyste chez RBC Capital Markets, anito-cel présente potentiellement un meilleur profil de sécurité, ce qui pourrait faire la différence auprès des oncologues hésitant à prescrire des traitements plus lourds sur le plan neurologique. C'est une course de vitesse où chaque mois de retard ou d'avance dans la commercialisation se compte en centaines de millions de dollars.
Stratégie de partenariats précoces : s'assurer l'exclusivité avant l'approbation
Cette opération met également en lumière une nouvelle tactique dans l'industrie : les partenariats précoces comme filet de sécurité. Il est important de noter que Gilead, via sa filiale spécialisée Kite Pharma, avait déjà établi un accord de collaboration avec Arcellx avant de procéder à ce rachat total. Ces partenariats agissent comme une sorte de droit de préemption, permettant aux grands groupes de surveiller de près une technologie prometteuse et de s'assurer qu'aucun autre prédateur ne s'y intéresse trop sérieusement.
Dans des domaines aussi concurrentiels que l'oncologie, où les enchères peuvent s'emballer très vite, disposer d'un pied à terre dans la capitale de la cible est un atout stratégique majeur. Cela permet à l'acquéreur de verrouiller la technologie, de connaître les détails des essais cliniques en interne et d'être prêt à déclencher l'offre de rachat dès que les données s'avèrent concluantes, et surtout, avant que la FDA, l'agence américaine du médicament, ne donne son feu vert définitif. Une fois le traitement approuvé, le prix de rachat de l'entreprise biotechnologique s'envole souvent, rendant l'opération moins rentable pour l'acquéreur. Gilead a donc joué finement en sécurisant la mise dès le début de la phase d'approbation réglementaire.

Un marché dominé par les acteurs asiatiques et américains
Il est également pertinent de noter que la concurrence dans ce secteur ne se fait pas seulement à l'échelle nationale, mais mondiale. Le partenariat entre Johnson & Johnson et Legend Biotech, une entreprise chinoise, illustre bien l'importance des acteurs asiatiques dans le domaine des thérapies cellulaires. La Chine est devenue un hub majeur pour l'innovation biotechnologique, capable de produire des traitements de classe mondiale à des coûts parfois plus compétitifs.
Face à cette alliance puissante, Gilead se devait de réagir pour ne pas perdre son leadership sur le marché américain. En acquérant Arcellx, le laboratoire s'assure non seulement une technologie de pointe, mais aussi une base de production et d'expertise située aux États-Unis. C'est un enjeu de souveraineté industrielle dans le domaine de la santé, où la maîtrise des technologies de pointe est devenue une question de sécurité nationale pour de nombreux pays. L'Europe, quant à elle, tarde un peu à se positionner sur ce segment spécifique, risquant de dépendre encore davantage des importations américaines et asiatiques pour ces traitements vitaux.
Une facture à 350 000 euros : qui payera les « miracles » de demain ?
Derrière les milliards de dollars échangés entre actionnaires et les promesses médicales extraordinaires se cache une réalité brutale : le prix exorbitant de ces thérapies pour le patient final. L'acquisition d'Arcellx par Gilead pour 7,8 milliards de dollars ne manquera pas d'impacter le coût de l'anito-cel. Il est donc légitime de s'interroger sur l'accessibilité de ces traitements miracles dans un monde où les systèmes de santé sont déjà sous tension financière. Le progrès scientifique a un prix, et c'est la société tout entière qui devra décider si elle est prête à le payer.
Le coût exorbitant du développement : 1 à 3 milliards par médicament
Avant de s'indigner du prix final d'un médicament innovant, il faut comprendre l'ampleur des risques et des investissements pris par les laboratoires. Selon les études les plus récentes, le coût moyen de développement d'un nouveau médicament oscille aujourd'hui entre 1 et 3 milliards de dollars. Ce montant astronomique couvre non seulement la recherche fondamentale et les essais cliniques, qui durent souvent plus de 10 ans, mais aussi l'échec de milliers d'autres molécules qui n'ont jamais passé le cap des essais.
L'acquisition d'Arcellx à 7,8 milliards de dollars inclut donc ces coûts passés, ainsi que l'anticipation des investissements futurs nécessaires pour finaliser les tests, produire les traitements à grande échelle et les commercialiser. Les investisseurs pharmaceutiques cherchent logiquement à rentabiliser ces mises de départ. C'est ce mécanisme économique complexe qui justifie des tarifs souvent jugés inacceptables par le grand public. Si l'on ne trouve pas un modèle économique viable pour financer cette recherche, l'innovation thérapeutique risque tout simplement de se tarir, laissant les patients sans espoir.

En France, le dilemme de la Sécurité sociale face aux 350 000 euros le traitement
Pour mesurer l'impact concret, il suffit de regarder le coût actuel des thérapies CAR-T en France. Des traitements comme Kymriah (Novartis) ou Yescarta (Gilead) sont facturés autour de 350 000 euros par patient. C'est une somme stratosphérique que la Sécurité sociale doit assumer, bien que le remboursement soit soumis à de strictes conditions d'éligibilité. La Haute Autorité de Santé (HAS) joue ici le rôle de gendarme, évaluant le « service médical rendu » pour tenter de négocier les prix à la baisse.
L'arrivée imminente de l'anito-cel va donc placer les autorités de santé françaises devant un dilemme impossible. Comment accepter de rembourser des traitements à ce coût sans sacrifier d'autres dépenses de santé ? Le risque est de voir se créer une médecine à deux vitesses, où les patients les plus aisés ou vivant dans des pays aux systèmes de santé riches auraient accès à ces innovations, tandis que les autres seraient laissés pour compte. Ce deuxième volet du « cancer » bancaire et mondial touche au cœur de notre modèle social : jusqu'où sommes-nous prêts à aller pour sauver une vie ?
Témoignage : quand la rémission a un prix inestimable mais une réalité complexe
Pour ne pas rester dans l'abstrait des chiffres, il est crucial de se rappeler que derrière chaque traitement se trouve un être humain. Prenons l'exemple de Sarane, atteinte d'un myélome multiple à seulement 46 ans. Après plusieurs rechutes et un échec thérapeutique total face aux traitements classiques, elle a reçu des cellules CAR-T en novembre 2018 au CHU de Nantes. Le résultat fut une rémission complète annoncée dès la fin de l'année, lui offrant une nouvelle vie qu'elle pensait perdue.
Son hématologue avait qualifié ce traitement de « chance unique ». Cette histoire émouvante met en lumière une ironie profonde : bien que la vie de Sarane soit inestimable, le traitement essentiel pour la sauver a un prix exorbitant. Son parcours illustre à la fois le potentiel réel de ces thérapies cellulaires et les dilemmes éthiques délicats concernant le montant de ces… « chances uniques » que la collectivité peut financer. À force de multiplier ces interventions à 350 000 euros ou plus, le système de santé risque l'implosion, créant une dissonance cruelle entre la capacité technique de sauver des vies et la capacité financière de le faire.
Vers 2028 : les prévisions de rentabilité et l'avenir des patients
Maintenant que la transaction est bouclée, tous les regards se tournent vers l'avenir. La date du 23 février 2026 marque le début d'une nouvelle ère pour Gilead, mais les fruits de cet investissement ne seront pas récoltés immédiatement. Les analystes et les investisseurs projettent désormais leurs calculs vers 2028, année charnière où l'anito-cel devrait atteindre son plein potentiel commercial et commencer à générer des retombées significatives, tant pour les actionnaires que, espérons-le, pour les patients désespérés de nouvelles options thérapeutiques.
Le pari sur l'approbation de la FDA : l'échéance de décembre 2026
La première étape critique de ce calendrier se situe le 23 décembre 2026. Ce jour-là, la Food and Drug Administration (FDA), l'agence américaine de régulation des médicaments, doit prendre sa décision finale concernant l'approbation de l'anito-cel en tant que traitement de quatrième ligne pour le myélome multiple. C'est le moment de vérité pour Gilead. Une validation par la FDA débloquerait non seulement le marché américain, le plus lucratif au monde, mais déclencherait aussi le paiement de la valeur résiduelle (CVR) de 5 dollars par action promise aux actionnaires d'Arcellx.
Cependant, l'incertitude règne toujours. Les procédures de la FDA sont rigoureuses et peuvent être imprévisibles. Un moindre doute sur la sécurité ou les données de fabrication pourrait repousser cette date ou, pire, entraîner un refus. C'est pourquoi Gilead a pris soin de ne pas tout miser sur ce seul produit. L'entreprise mise sur la diversité de son pipeline pour absorber le choc si nécessaire. Mais pour l'instant, tous les espoirs de l'opération Arcellx reposent sur ce feu vert administratif qui viendra sanctionner des années de recherche et 7,8 milliards de dollars d'investissement.

Effet relutif en 2028 : quand le business rejoint la médecine
Les prévisions financières des analystes, comme Evan Seigerman de BMO Capital Markets, tablent sur un « effet relutif »… dès 2028. Ce critère financier indique que l'acquisition devrait, à terme, accroître le bénéfice par action de Gilead au lieu de le diluer. En clair, à partir de 2028, l'anito-cel ne constituera plus un fardeau financier, mais deviendra une source de revenus pour le groupe. Les experts anticipent que ce traitement est destiné à s'imposer comme un… « produit de plusieurs milliards de dollars », rivalisant directement avec Carvykti.
Cette perspective financière est bonne nouvelle pour les investisseurs, mais elle l'est aussi pour les patients. Pour que Gilead gagne de l'argent, il faut que l'anito-cel soit prescrit largement et utilisé sur des milliers de malades à travers le monde. Le succès financier des laboratoires est donc intrinsèquement lié au succès médical des patients. C'est une rare convergence d'intérêts où la recherche du profit maximal pousse l'industrie à développer les traitements les plus efficaces possibles. Reste à savoir si les systèmes de santé pourront suivre ce rythme effréné d'innovation et d'investissement sans sacrifier l'équité de l'accès aux soins.
L'expansion potentielle vers les lignes de traitement précoces
À plus long terme, l'ambition pour l'anito-cel ne s'arrête pas au traitement des patients en rechute multiple. Si les résultats de sécurité se maintiennent, Gilead pourrait viser des lignes de traitement plus précoces, c'est-à-dire administrer la thérapie CAR-T dès les premiers stades de la maladie, avant que les patients ne soient épuisés par la chimiothérapie. C'est ce qu'on appelle le « treatment earlier », une stratégie qui permettrait d'augmenter considérablement le nombre de patients éligibles.
En se déplaçant vers la première ou la deuxième ligne de traitement, le marché potentiel d'anito-cel pourrait exploser. Cependant, cela implique de nouvelles études cliniques et des défis supplémentaires en termes de risque-bénéfice, car on demande alors un profil d'innocuité encore plus parfait pour des patients qui ont encore des options thérapeutiques standards. C'est l'étape suivante, cruciale pour maximiser le retour sur investissement des 7,8 milliards de dollars dépensés, et qui pourrait redéfinir le standard de soins du myélome multiple pour la prochaine décennie.

Conclusion : Le pari de l'avenir entre espoir scientifique et défis éthiques
L'acquisition d'Arcellx par Gilead pour 7,8 milliards de dollars illustre parfaitement la dualité de la médecine moderne. D'un côté, elle représente une avancée technologique extraordinaire, capable de sauver des vies considérées comme perdues il y a encore quelques années. De l'autre, elle cristallise les tensions économiques d'un modèle de santé qui repose sur des investissements colossaux et une rentabilité à très long terme. Le défi pour les années à venir ne sera pas tant scientifique que politique et éthique.
Daniel O'Day, le PDG de Gilead, a résumé la situation en affirmant que cet accord témoignait de la « volonté d'agir rapidement » pour les patients. Cependant, cette urgence se heurte à la dure réalité des coûts. Si des vies seront incontestablement sauvées grâce à l'anito-cel, le modèle économique actuel risque de consolider une médecine à deux vitesses. L'accès à ces innovations dépendra moins du besoin médical urgent d'un patient que de la solvabilité de son système de santé ou de sa couverture d'assurance. Comme le soulignent les inquiétudes autour des factures à 350 000 euros, la sortie du déni sur ces enjeux est nécessaire pour éviter une fracture sanitaire majeure.
En définitive, le pari fou de Gilead sur Arcellx est un miroir tendu à notre société. Il reflète notre capacité d'innovation sans précédent, mais aussi notre difficulté à répartir équitablement les fruits de cette innovation. Entre l'espoir médical prodigieux offert par les thérapies cellulaires et le risque d'une exclusion médicale fondée sur l'argent, le chemin étroit de l'avenir reste à tracer. L'année 2028 et celles qui suivront diront si nous avons réussi à concilier le business de la santé et le droit à la vie pour tous.